Konkrete redskaber og eksempler
Oplever du som læge at være involveret i processer, der burde køre bedre? Har du oplevet skade på patienter, som kunne være forebygget?
Har du lyst til at bruge de data, der indtastes i millionvis i vores elektroniske systemer og finde mønstre og sammenhænge, der kan forbedre patientbehandlingen?
Læge - kend din kvalitet giver dig redskaber, så du kan komme i gang med at forbedre processer og arbejdsgange og øge kvaliteten af patientbehandlingen.
Bogen er skrevet af læger med erfaring indenfor kvalitetsudvikling og forbedringsarbejde, og indeholder en række eksempler.
Forord af Kira Ørbekker, patientambassadør og sygeplejerske
Da min svigermor brækkede hoften, var hun igennem et meget fragmenteret forløb i sundhedsvæsenet. I løbet af et døgn var hun indlagt på tre forskellige afdelinger. Ikke hensigtsmæssigt for en ældre kvinde med begyndende demens. Hun var urolig under indlæggelsen og blev behandlet med Serenase, som hun også fik med hjem ved udskrivelsen, først til et korttidscenter og derefter til hjemmet.
Hjemme igen var det min svigerfar, som er en virkelig frisk mand, der skulle administrere medicinen. Det er han ikke vant til, og han tog han fejl af laktulose og Serenase. På et tidspunkt var han ved at give hende 20 ml Serenase i stedet for laktulose. Han tænkte ikke over navnet, for medicin skifter jo navn hele tiden. Og egentlig skulle hun slet ikke have haft Serenase med hjem, for hun havde ikke brug for det.
Hun fik infektion i hoften og blev afvist flere gange ved lægevagten, men endte med at blive indlagt igen. Hendes tilstand var kritisk, og hun kom i respirator. Hospitalet aftalte med min svigerfar, at han ville komme til en samtale om det videre forløb ved middagstid. Men i løbet af formiddagen slukkede de for respiratoren, uden at han havde nået at få besked, og hun døde alene.
Som patient og pårørende oplever man ikke altid, at der er sammenhæng i sundhedsvæsenets arbejde. Der er mange samarbejdspartnere, som egentlig ikke snakker særligt meget sammen, og der er manglede forståelse for hinandens virkelighed.
For at styrke denne sammenhæng har vi brug for lægernes indsats. Lægerne har behandlingsansvaret, de har autoriteten, og det er dem, der har de tværgående kontakter og kan være gennemgående personer i behandlingsforløbet.
Som plejepersonale kan vi godt have en hel masse gode ideer, men vi når ikke i hus, hvis ikke vi har lægerne med. Det er lægerne, der kan hjælpe til at skabe de glidende overgange. Når en patient sendes videre i systemet, hvem har så ansvaret for behandlingen, og hvad er planen med den opgave, der er sat i gang.
Det er mit håb, at denne håndbog kan være med til at inspirere læger til at gå foran i kvalitetsudvikling og forbedringsarbejde, for at vi som patienter og pårørende kan få oplevelse af sammenhæng, af at alle trækker i samme retning, og at forløbene bliver mindre fragmenterede.
God læselyst
Kira Ørbekker, sygeplejerske og medlem af Patientambassadørerne, et netværk af patienter og pårørende, der arbejder for et sikkert og effektivt sundhedsvæsen.
Forord af redaktionsgruppen
Kære kollega
Velkommen til en webbaseret håndbog udviklet af læger for læger, der ønsker at medvirke til at forbedre kvaliteten i sundhedsvæsnet til gavn for patienterne.
Patienterne har legitime krav på individualiseret behandling af høj faglig kvalitet. Med nye teknologier, en fremtid med langt flere ældre og stadig mere evidens for flere behandlingsmuligheder for flere tilstande, kan vi se frem til, at kompleksiteten i sundhedsvæsnet øges og at færre medarbejdere skal behandle flere patienter for mere. Det kræver mange løbende tilpasninger og nytænkning af patientforløbene for ikke at gå ud over kvaliteten.
Her er lægerne vigtige, hvis nye arbejdsgange skal udvikles med udgangspunkt i den højeste faglighed.
Læger har ikke indflydelse på alle arbejdsgange i sundhedsvæsnet: Fremtidens sundhedsvæsen stiller også store krav til ledere, der har fokus på den faglige kvalitet, patienternes oplevelser, fornuftig anvendes af ressourcerne og arbejdsglæden.
Men mange dagligdags arbejdsgange har læger direkte indflydelse på. Vi håber, at denne hjemmeside kan medvirke til at vise jer, hvordan I kan påvirke arbejdsgangene, og at det i den sidste ende vil være til stor gavn for patienterne, kollegerne og dermed også arbejdsmiljøet.
Indholdet på hjemmesiden er en blanding af teorier, metoder og erfaringer, der kan anvendes som afsæt for at analysere kvalitetsproblemer, forstå arbejdsgange, hvordan man forbedrer dem og dermed, hvordan man som læge kan medvirke til at sikre, at best practice og evidensbaserede behandlinger bliver systematisk implementeret og kommer patienterne til gavn.
Mange læger har af sig selv til alle tider – uden behov for hjemmesider eller teorier - forbedret arbejdsgange i sundhedsvæsnet.
For dem er erfaringerne her nok ikke noget nyt. For denne gruppe kan hjemmesiden dog måske give et sprog til at dele erfaringer med andre. Desuden håber vi, at hjemmesiden måske kan give inspiration til, hvordan man kan publicere sine resultater og dermed medvirke til at lære fra sig – og få anerkendelse for det arbejde man udfører.
Redaktørerne og forfatterne til indlæggene på hjemmesiden er alle læger, der selv har erfaring med at gennemføre forbedringsprojekter typisk på sygehusene og i psykiatrien. Men metoderne og erfaringerne kan anvendes af alle faggrupper og bredt i hele samfundet.
Det er Dansk Selskab for Patientsikkerhed og Regionernes Kliniske Kvalitetsudviklingsprogram, der i fællesskab står bag hjemmesiden.
Som andre hjemmesider er resultatet ikke statisk. Og vi håber, at du vil bidrage til at udbygge den med dine erfaringer og feedback. Se kontaktoplysninger i bunden af siden.
God læselyst!
Louise Rabøl
Jens Winther Jensen
Jacob Anhøj
Charlotte Frendved
Introduktion
 Hvorfor er det vigtigt, at alle kan forbedre?
Hvorfor er det vigtigt, at alle kan forbedre?
Af Louise Rabøl, ledende overlæge, Øre-, Næse-, Hals- og Kæbekirurgisk Afdeling, Sjællands Universitetshospital
Læger er traditionelt godt uddannet til at medvirke til forskning: Vi har tidligt på medicinstudiet lært om randomisering, kontrolgrupper, etiske overvejelser og p-værdier. Vi er ovenikøbet en del af et system, der i høj grad anerkender forskning, når vi skal tildeles stillinger, uddannelser og hædersbevisninger.
Men den anden del af processen – at implementere forskningsresultaterne og sikre, at de ikke kun havner på side 354 i et videnskabeligt tidsskrift, men at de gennem nye arbejdsgange bliver en del af den kliniske hverdag og kommer alle relevante patienter til gavn – har vi som læger langt mindre teoretisk og praktisk viden om.
Hvad vil du gerne forbedre?
Af Julie Mackenhauer, læge, ph.d.
Ideer til, hvad du gerne vil forbedre, kan opstå i mange sammenhænge. Mange ideer kommer fra personlige oplevelser. En fejl, en klage eller et forløb du har været involveret i, som burde have været endt på en anden måde. Ideer kan også komme fra din dagligdag, som er præget af processer der burde køre bedre eller i et andet tempo. Du kan opleve en fortvivlelse eller indignation over, hvorfor systemet ikke præsterer bedre – et dødsfald som burde være undgået eller en skade på en patient, som kunne være forebygget.
Ideer kan også opstå fra en social samvittighed eller et samfundsøkonomisk ønske om, at ressourcerne burde fordeles bedre. Du kan have en lyst til at bruge alle de data, der hver dag indtastes i millionvis i vores elektroniske systemer - finde mønstre og sammenhænge, der kan forbedre patientbehandlingen eller sundhedsplanlægningen. Måske har du talt med en kollega et sted i Danmark eller et sted i verden som arbejder med det samme som dig – bare mere effektivt eller med bedre resultater for patienten og personalet?
Datakilder, der kan bidrage til analyser af kvaliteten
Af Julie Mackenhauer og Charlotte Frenved
Analyseværktøjer
Af Julie Mackenhauer
Brug af data og "pakker" i kvalitetsudvikling
Af Jens Winther Jensen, læge, MPH, direktør, Regionernes Kliniske Kvalitetsudviklingsprogram
I traditionel evidens genererende forskning, hvor formålet er at dokumentere ny viden om en behandlings effekt, er der ofte brug for randomiserede, kontrollerede undersøgelser af tilstrækkeligt store, repræsentative populationer. Ellers bliver konklusionen ikke sikker nok.
I forbedringsarbejdet er behovet for data anderledes. Her drejer det sig om, hvordan arbejdsgangene kan indrettes, så patienten med sikkerhed modtager de evidensbaserede ydelser. Altså typisk implementering af en allerede kendt behandling hvor evidensen er beskrevet.
Går du ud og kigger på fem patienter og opdager, at der er mangler i plejen eller behandling hos tre af dem, så behøver du ikke at undersøge, om de fem patienter er repræsentative for den samlede patientpopulation. Det kan med det samme konstateres, at arbejdsprocessen ikke er robust, og at der er behov for forbedring. I stedet for at fortsætte målingerne, vil du ofte få mere ud af at studere de fem patientforløb nærmere og undersøge, hvad der gik godt, og hvad der gik skidt.
Eksempler fra forbedringsarbejdets historie
Af Jacob Anhøj, overlæge, Diagnostisk Center, Rigshospitalet
Forbedringsarbejde har en lang og interessant forhistorie, som involverer betydningsfulde personer og banebrydende ideer, som har været med til at forme kvalitetsforbedringsmetode som håndværk og videnskab.
Forbedringsmodellen
 Forbedringsmodellen
Forbedringsmodellen
Af Charlotte Frendved, læge, faglig redaktør, Dansk Selskab for Patientsikkerhed
Forbedringsmodellen er generisk og kan bruges bredt i kvalitetsudviklingen. Det er en dynamisk model, der betyder, at man efterhånden opnår viden, og undervejs kan tilrette sin projektplan i forsøget på at opnå en højere kvalitet.
Ligesom den kliniske og den forskningsmæssige videnskabelige tankegang er forbedringstankegangen også en videnskab, og den indebærer en systematik, der skal læres.
Forbedringstankegangen bygger på Demings arbejde, der er videreudviklet til brug i sundhedsvæsenet af en gruppe amerikanske akademikere, primært statistikere, der kalder sig Associates in Process Improvement (API).
Hvad ønsker vi at opnå?
Af Ole Bredahl Rasmussen, overlæge, Gynækologisk-Obstetrisk Afdeling, Hospitalsenheden Vest
Et af de tre spørgsmål i forbedringsmodellen handler om, at du skal sætte dig mål for, hvad du ønsker at opnå. Det lyder umiddelbart let, men det kan være svært at formulere præcist. Er målet ikke veldefineret, kan det være vanskeligt at vide, hvilke handlinger der skal afprøves og iværksættes, samt vanskeligt at måle, om de indførte forandringer er en forbedring.
Forbedringsmodellen anbefaler, at du så vidt muligt altid opstiller numeriske mål for forbedringsinitiativer, og at du fastsætter en tidsramme. Det er altså ikke nok at sige, at man vil forbedre kvaliteten for patienterne. Målet skal beskrive: Hvad? Hvor meget? Hvornår? For hvem?
Hvornår ved vi, at en forandring er en forbedring?
Af Jacob Anhøj, overlæge, Diagnostisk Center, Rigshospitalet
og Charlotte Frendved, læge, faglig redaktør, Dansk Selskab for Patientsikkerhed
Som oftest har du brug for data, når du skal svare på det andet spørgsmål i forbedringsmodellen: ”Hvornår ved vi, at en forandring er en forbedring?”. Med data kan du fastlægge dit udgangspunkt (baseline), du kan følge med i, om dine forbedringstiltag har den ønskede effekt, og i sidste ende, om du når det mål, du har sat dig.
I kvalitetsarbejdet er det vigtigt, at data er friske og afspejler den aktuelle status, og at data opgøres hyppigt, så du kan følge dem fra dag til dag eller fra uge til uge. De færreste er motiverede af at arbejde med kvalitetsforbedringer, hvis de kun har få datapunkter til rådighed, og de måske endda er fra sidste år.
Noget andet karakteristisk ved forbedringsarbejdet er, at data anvendes som motiverende og visuelt værktøj, og ofte hænges op på en ”forbedringstavle”, der er synlig for hele afdelingen. Et seriediagram, som viser data dag for dag, er intuitivt nemt at forstå. Det er let at se, hvor langt vi er fra det mål, vi har sat os, og om forbedringsarbejdet giver resultater.
Hvilke forandringer kan iværksættes for at skabe forbedringer?
Af Charlotte Frendved, læge, faglig redaktør, Dansk Selskab for Patientsikkerhed
og Ann Lyngberg, ledende overlæge, ph.d., Arbejds- og Socialmedicinsk Afdeling, Holbæk Sygehus
Dette spørgsmål i forbedringsmodellen handler om at indkredse de forandringsideer, som du vil prøve af. I forbedringsarbejdet låser du dig ikke fast på bestemte løsninger fra starten. Ideer udvikles, tilpasses undervejs, nogle ideer forkastes og andre opstår i processen.
På den måde adskiller forbedringstankegangen sig fra den klassiske forskningsmetode i lægevidenskaben, hvor man på forhånd definerer sin intervention. Men ligesom ved de traditionelle lægelige arbejdsmetoder, beskriver du nøje din proces og dine tiltag undervejs, sådan at andre kan lære af det.
PDSA-cirklen: Afprøvning og tilpasning
Af Charlotte Frendved, læge, faglig redaktør, Dansk Selskab for Patientsikkerhed
PDSA er forbedringsmodellens motor til at omsætte forbedringsideer til konkrete handlinger. En PDSA-cirkel indebærer, at du planlægger, hvad du vil afprøve, du går ud og gør det, analyserer resultatet af afprøvningen og bruger denne analyse til at planlægge næste afprøvning.
Når du arbejder med PDSA, skal du starte småt – meget mindre end du måske umiddelbart har lyst til. En første afprøvning kan således med fordel afprøves på én patient én gang med en kollega. Efterhånden kan du gøre afprøvningerne større og større – flere kollegaer – flere patienter – over længere tid.
Fordelen ved at starte i lille skala er, at du kan tilpasse din ide til den praktiske virkelighed, inden du implementerer i større skala. Ideer, der er vanskelige at gennemføre, kan forkastes uden de store omkostninger. Med PDSA får du hurtigt svar på, hvordan din ide virker i praksis, og cirkel for cirkel kan du kredse dig ind på den mest optimale løsning.
Kom godt i gang
 Kom godt i gang
Kom godt i gang
Af Ann Lyngberg, ledende overlæge, ph.d., Arbejds- og Socialmedicinsk Afdeling, Holbæk Sygehus
Der er en række praktiske forhold, som du skal tænke på, når du starter et nyt projekt, da de er vigtige for, at arbejdet med projektet kan få succes. Hvordan sammensættes fx et forbedringsteam mest optimalt? Hvordan tilrettelægges teamets arbejde bedst muligt? Hvordan kan du inddrage kolleger og samarbejdspartnere? Hvordan bevarer I motivationen?
Organisering af større projekter
Af Ole Bredahl Rasmussen, overlæge, Gynækologisk-Obstetrisk Afdeling, Hospitalsenheden Vest
Hvis du ikke har erfaring med kvalitetsudviklingsprojekter, er det en god ide at begynde med et mindre afgrænset projekt. Men efterhånden som du får greb om metoderne, kan du kaste dig over større og mere komplekse opgaver.
Med et større projekt menes fx kvalitetsudvikling, der involverer mange sammenhængende arbejdsgange og dermed flere afdelinger, flere specialer eller flere faggrupper, sådan at der er brug for mere overordnet koordinering på tværs. Det kan også dreje sig om projekter, der er ressourcekrævende i form af materialeanskaffelser eller forbrug af arbejdstid. Disse store projekter kræver planlægning fra starten, og de kræver en høj grad af ledelsesinvolvering.
Sådan får du hjælp fra din ledelse
Af Mads Koch Hansen, læge, rådgiver, ledelsescoach
Hvad gør du som læge, hvis du står med en klinisk problemstilling, som tydeligvis trænger til at blive arbejdet med?
Det endelige ansvar for kvaliteten i et patientforløb og dermed for kvalitetsarbejdet ligger selvfølgelig hos afsnitsledelsen, afdelingsledelsen og hospitalsledelsen.
Men din ledelse er travle folk, så du kan med fordel forberede dig, så du øger sandsynligheden for, at ledelsen prioriterer ’din problemstilling’. Det er således en fordel, at du beskriver din problemstilling og finder relevante alliancepartnere, inden du går i dialog med din ledelse.
Begynderfejl, vi alle har prøvet
Af Jens Stubager Knudsen, overlæge, Bedøvelse og Intensiv, Sygehus Lillebælt
Hvis du får ideen til et forbedringsprojekt, der virkelig vil betyde noget for patientbehandlingen i din dagligdag, er det langt fra sikkert, at du opnår det resultat, du havde forestillet dig. Der er mange trin, hvor der er mulighed for at begå fejl, som enten forsinker dit projekt unødigt eller umuliggør gennemførslen.
De fleste fejlmuligheder kan dog forebygges, hvis du sætter dig grundigt ind i emnet, sætter fornuftige mål, får opbakning fra din ledelse, inddrager relevante kolleger, der skal udføre forbedringerne, indsamler tilstrækkelige data og starter alt i lille skala, hvor du kan lære af dine fejl med ringe konsekvenser for patienterne.
Hensigten med dette kapitel er at du kan lære af de fejl, dine forgængere har begået, så du nemmere kan gennemføre dit forbedringsprojekt.
Publicering
 Publicering af kvalitetsforbedringsarbejdet
Publicering af kvalitetsforbedringsarbejdet
Af Ole Bredahl Rasmussen, overlæge, Gynækologisk-Obstetrisk Afdeling, Hospitalsenheden Vest
Alle, der arbejder i sundhedsvæsenet, har en etisk forpligtelse til at levere bedst mulig behandling, hvilket også indebærer, at vi diskuterer vores arbejde med andre professionelle (1). Og så er det er spild af ressourcer og tid at opfinde den dybe tallerken mere end én gang. På samme måde skal man beskrive og fremlægge kvalitetsforbedringsarbejde, så de gode ideer kan prøves af andre og dermed komme endnu flere patienter til gode - uden at skulle opfindes fra bunden hver gang. Selv hvis en ny intervention ikke har medført den intenderede forbedring, vil der kunne være værdifuld viden om processer og kontekst at lære fra et givet forløb.
Der er brug for, at al den viden om implementering af nye arbejdsgange, der indhentes i arbejdet med kvalitetsforbedring, gøres så videnskabelig som muligt, beskrives videnskabeligt og publiceres i videnskabelige sammenhænge. Vi har en overordnet mission inden for kvalitetsforbedring med at demonstrere, at kvalitetsforbedringsarbejde ikke bare er noget, der kan handles af med et hurtigt møde på gangen eller med ”ølregnskaber” og streger på et stykke papir.
Dermed ikke være sagt, at hurtige møder og stakitter ikke kan være brugbare og effektive som integrerede dele af et projekt. Men arbejdet med kvalitetsforbedring er en videnskab, som gør krav på samme respekt og faglige værdsættelse som traditionel videnskab (2). Jo mere vi øver os i den stringente tankegang, der er nødvendig for at kunne publicere, jo mere virker det tilbage på vores praksis og forbedrer vores evne til at forestå kvalitetsforbedringsprojekter. På det personlige plan tæller det naturligvis med, at publikationer kan sættes på ens CV.
For at det skal lykkes, bør man i ethvert kvalitetsforbedringsprojekt fra starten forholde sig til muligheden for at publicere sit projekt i et internationalt fagfællebedømt tidsskrift.
Er kvalitetsforbedringsarbejde videnskab?
Man bliver ofte mødt med en påstand om, at kvalitetsforbedringsarbejde ikke er videnskab, fordi det jo ikke handler om at udvikle ny viden om, hvordan en given sygdom skal behandles. Kvalitetsforbedringsarbejde handler i princippet om at opnå ny viden om, hvordan viden rent faktisk bliver implementeret i en given kontekst.
Men kvalitetsforbedringsarbejde kan også foregå på planlagt, systematisk måde med fremskaffelse af objektive data til analyse af virkeligheden, så vi kan ændre på den i den ønskede retning. Dette er i princippet ikke forskelligt fra anden videnskab. Stringent kvalitetsforbedringsarbejde kan foregå både inden for forebyggelse, diagnostik og behandling.
Hvis et kvalitetsforbedringsprojekt beskrives i et charter (svarende til en protokol for et forskningsprojekt), bliver dokumenteret fortløbende og afrapporteret i henhold til givne standarder, så kan kvalitetsforbedringsarbejde også opfattes som videnskab. Hvis man desuden i et forløb med et projekt registrerer de enkelte elementer i den nye intervention detaljeret, vil man også kunne anvende data til en efterfølgende analyse og dermed ovenikøbet generere ny viden om selve behandlingen.
Case: Færre alvorlige læsioner hos fødendeI projektet registrerede forbedringsteamet brugen af hvert element i interventionen ved hver fødsel. Det har vist sig, at der i dette forbedringsprojekt er registreret langt mere detaljeret, end det er gjort i andre tidligere publicerede observationelle studier samt i de alle de randomiserede studier, der findes på området. I de traditionelle publikationer redegør man ikke for, hvad der rent faktisk blev gjort ved fødslerne, hverken i den "arm" af studiet, hvor der ikke skulle ske en intervention (hands-off), eller i den ‘arm’, hvor der skulle interveneres (hands-on). I realiteten ved man ud fra publikationen ikke, om behandlingen i de to arme reelt var forskellige, hvilket kan forklare, hvorfor RCT´erne ikke kan vise forskelle. Fokus på nøje registrering af procesindikatorer kan generere helt ny viden. |
I realiteten kan det dog i en given situation være vanskeligt at afgøre, om et projekt skal kaldes forskning eller kvalitetsforbedring. Projektets status kan have indflydelse på, hvilke rettigheder og pligter, der er gældende ift. indhentning og opbevaring af data fra den elektroniske patientjournal.
Man kan skele til følgende forhold (reference: Michigan University, USA), som alle peger i retning af, at projektet skal betragtes som traditionel forskning med deraf følgende pligter ift. godkendelse og dataopbevaring:
- Er patienterne randomiseret til forskellige interventioner?
- Skal der undersøges forhold som er nye ift. i forvejen kendt viden og erfaring?
- Er de involverede forskere uden behandlingsmæssige forpligtelser ift. afdelingens patienter?
- Er protokollen ”låst” – dvs. at den ikke kan eller må ændres i forløbet af projektet?
- Vil der være forsinket eller slet ingen feedback til klinikerne og patienterne i projektet?
- Er der en udefra kommende sponsor, som evt. kan have en interesse i resultaterne?
Er man trods dette usikker på, hvorledes et projekt skal defineres, bør man diskutere det lokalt og evt. afklare ved at ansøge Videnskabsetisk Komite. Komiteen tager stilling til, om godkendelse er nødvendig. Selv om godkendelse ikke er nødvendig, er afgørelsen fra komiteen god at sende med til tidsskriftet, når man ønsker at publicere.
To typer kvalitetsforskning
”Der findes to hovedtyper af kvalitetsforbedringsarbejder. Den ene handler om at indføre en ”pakke” – en såkaldt care bundle. Den anden handler om at optimere en given behandling eller patienthåndtering ift tid.
1) Ideen med den første type projekt er at de forskellige kendte elementer indføres samtidigt og koordineret og hvor brugen af hvert enkelt element dokumenteres for hver enkelt patient. Et godt eksempel herpå er indførelsen af Tryksårspakken i det nationale projekt ”I Sikre Hænder”. Ud over at sikre god kost og tilstrækkelig væske er der en række andre elementer, som man skal forholde sig til (www.isikrehaender.dk hvor man kan finde dokumentation og omtale af Tryksårspakken).
”En sådan samlet vurdering af flere evidensbaserede områder kaldes på engelsk et Care bundle, som vil føre til et væsentligt bedre resultat frem for enkelte indsatser (National klinisk retningslinje for Forebyggelse af Tryksår hos voksne over 18 år. Sundhedsstyrelsen September 2020)”.
Evidensen for at denne type interventioner har en kausal betydning for et bedre udkomme vil oftest hvile på undersøgelser af de enkelte elementer.
2) Ideen med den anden type projekt er at forbedre et tidsforbrug, fx i forbindelse med akut indlæggelse til undersøgelse og akut behandling ved apopleksi eller det tidligere beskrevne projekt til optimering af akutte kejsersnittider i Herning og Holstebro (nu Gødstrup) – se side 81. For de mest akutte og alvorlige situationer vil det oftest ikke være muligt at skaffe den højeste grad af evidens for at fx hurtigere kørsel til hospitalet eller til forløsning forbedrer overlevelse og førlighed for patienten, da det vil være uetisk at bruge tid i situationen på at indhente informeret samtykke til deltagelse i en randomiseret undersøgelse. Derudover vil det byde alle imod, at den ene arm i en evt randomiseret undersøgelse skulle udføres langsommere end det er muligt. Denne type forbedringsprojekt vil ofte involvere flere faggrupper, specialer, afdelinger og evt sektorer.
Evidensen for at denne type intervention medfører et bedre udkomme vil ofte hvile på observationelle studier samt en intuitiv opfattelse af best practice.
Forskning i implementeringsmetoderDer er eksempler på initiativer, der skal skabe evidens for implementerings og forbedringsmetoder. Fx oprettede den britiske fond Health Foundation i 2018 The Healthcare Improvement Studies Institute, THIS Institute (8). Tankegangen er, at når vi stræber efter at forbedre pleje og behandling, skal disse bestræbelser bygge på evidensbaserede metoder. THIS arbejder for at skaffe klarhed over, hvilke implementeringsmetoder der virker, og hvilke der ikke gør. |
Hvad skal man huske fra starten, hvis man vil publicere?
Den stringente tankegang, der er nødvendig for at publicere, skal starte allerede i den indledende fase af projektet, hvor du udarbejder charteret, der fungerer som den grundlæggende projektbeskrivelse eller protokol.
Samtidig kan du med stor fordel oprette en dagbog over fremdriften. Alle vigtige beslutninger, aftaler og interventioner – herunder PDSA´erne – skal noteres kronologisk, så du senere kan finde tilbage og præcist beskrive forløbet i projektet og hvilke forhold, som på det givne tidspunkt var årsag til handlingen. Man skal kunne anføre den slags på det rigtige sted som annotationer i et serie- eller kontroldiagram, hvorved udviklingen i projektet kan beskrives i oversigtsform og den kausale sammenhæng kan diskuteres. Kronologien er således central for beskrivelse af projektet. Derudover skal man kunne dokumentere, hvor og hvordan data er indsamlet, behandlet og analyseret.
Hvis man vurderer, at man har behov for personhenførbare data, skal der søges tilladelse fra Datatilsynet. Dette gøres fra regionernes hjemmesider. Data skal naturligvis opbevares og håndteres korrekt i henhold til instrukser for dette. Hvis man har interesse i, at projektet skal munde ud i en publicering, vil det kunne gøre det lettere, hvis man får en forhåndsgodkendelse fra den lokale videnskabsetiske komite. Svaret vil typisk være, at der ikke kræves godkendelse fra en videnskabsetisk komite, da projektet beskrives som et kvalitetsforbedringsprojekt. Det er dette svar, der ofte efterspørges fra tidsskrifterne. De regler, der gælder på området, kan blive ændret eller gjort mere specifikke. Det er derfor vigtigt, at man undersøger dette konkret.
Ligeledes bør man fra starten af et projekt forholde sig til "The SQUIRE Guidelines" for rapportering af kvalitetsforbedrings arbejde – formålet med disse guidelines er: ”... to promote excellence in healthcare improvement reporting”, se tabellen nedenfor.
Revised standards for Quality Improvement Reporting Excellence (SQUIRE 2.0) Publication Guidelines (9)
Title and Abstract
Indicate that the manuscript concerns an initiative to improve health care (broadly defined to include the quality, safety, effectiveness, patient-centeredness, timeliness, cost, efficiency, and equity of health care)
Introduction - Why did you start?
Description Nature and significance of the local problem.
Summary of what is currently known about the problem, including relevant previous studies.
Informal or formal frameworks, models, concepts, and/or theories used to explain the problem, any reasons or assumptions that were used to develop the intervention(s), and reasons why the intervention(s) was expected to work.
Purpose of the project and of this report Methods - What did you do?
Contextual elements considered important at the outset of introducing the intervention(s)
Ethical aspects of implementing and studying the intervention(s) and how they were addressed, including, but not limited to, formal ethics review and potential conflict(s) of interest Results - What did you find?
Discussion - What does it mean?
Sources of funding that supported this work. Role, if any, of the funding organization in the design, implementation, interpretation, and reporting. På hjemmesiden for EQUATOR (10) findes opdaterede referencer og yderligere oplysninger med fortolkninger af nøgleord og begreber. |
Jo mere omhyggelig man er med de formelle dele af sit projekt som fx et gennemarbejdet charter, driverdiagram, arbejdsgangsanalyse og en præcist beskrevet måleplan, desto mere ligetil er projektet at udføre, og jo enklere er det at rapportere projektet på et videnskabeligt niveau mhp. publikation i et internationalt tidsskrift.
Tre forskellige forhold fortjener særlig opmærksomhed ift. publicering af kvalitetsforbedringsarbejde:
Det første er selve det rationale – eller teorien bag – som førte til forbedringsprojektet. Hvad findes der i forvejen af viden på området? Dette skal forstås helt bredt i form af randomiserede undersøgelser, observationelle studier, konsensusrapporter og guidelines. Desuden bør man sætte sig ind i, hvad andre gør og gerne opsøge andre afdelinger for at få gode ideer og direkte informationer og kontakter til brug for et projekt i egen afdeling. Husk selvfølgelig altid at give behørig kredit til de personer eller afdelinger, som er gået foran med de gode ideer, som ligger til grund for dine egne.
For det andet skal man i et kvalitetsforbedringsprojekt gøre særlig meget ud af at beskrive den specifikke kontekst, hvori projektet finder sted. Det kan virke vanskeligt for mere ”traditionelt skolede” forskere, som lidt firkantet sagt er trænet i at finde frem til en behandling, som vil virke ”alle steder og for alle mennesker og til alle tider”. Med andre ord skal man i traditionel forskningssammenhæng forsøge at fjerne betydningen af den specifikke kontekst på behandlingen. I kvalitetsforbedringssammenhæng skal konteksten tværtimod erkendes og beskrives inklusive den betydning, den kan tænkes at have på projektets fremdrift og eventuelle succes (11).
Vurdering af kausalitet
For det tredje skal man forholde sig til, om man kan tilskrive interventionen kausalitet ift. resultatet. Kvalitetsforbedringsprojekter er typisk designet som observationelle, prospektive, ’før versus efter’ undersøgelser. Dvs. at man opsamler data fra før en intervention og sammenligner med data, efter at interventionen er sat i værk og undervejs i projektet. Som altid ved observationelle (og andre) studier er bias og confounding udfordrende at holde styr på. Det kræver indsigt i de faglige forhold og den specifikke kontekst, hvori projektet finder sted.
Der kan være en for kort eller ikke-repræsentativ baseline, hvilket i sig selv kan forklare både succes med projektet eller manglende succes. Tilfældigheder eller andre projekter som iværksættes samtidig, kan have indflydelse på udfaldene. Der kan være særlige gunstige eller ugunstige forhold på den specifikke afdeling (konteksten), som har betydning for succes. Hvis man vælger straks at starte sit projekt og dermed sin intervention, før man opnår en baseline før interventionen, vil det kunne nedsætte muligheden for at kunne vise en effekt. Omvendt kan det hjælpe til at komme i gang, så man ikke skal afvente en langsommelig indhentning af baselinedata, hvor den nye intervention måske alligevel vil blive taget i brug, fordi rygterne om den vil sprede sig i afdelingen.
Det er naturligvis for alle implicerede og ift. den videre udbredelse af resultaterne ("spread") langt mere overbevisende, hvis man kan sandsynliggøre et kausalt forhold mellem intervention og et positivt resultat. Det er ikke muligt (og nok heller ikke ønskeligt), at enhver intervention skal afvente resultater fra en randomiseret kontrolleret undersøgelse (RCT) til at afklare dette spørgsmål. Dertil er de alt for dyre og tidsmæssigt krævende at gennemføre ift. alle de mange relevante spørgsmål, der opstår i klinikken. En RCT i sig selv er heller ikke nødvendigvis garanti for korrekte konklusioner. Fx kan der være manglende randomisering i randomiserede undersøgelser af af håndgreb (12) (13).
I kvalitetsforbedringsprojekter kan sammenhængen mellem interventionen og resultatet diskuteres og vurderes på baggrund af Bradford Hill Criteria (14), som gennemgår ni forskellige aspekter af association, der tilsammen kan hjælpe til en vurdering af styrken af kausalitet. Se nedenfor en gennemgang af casen "Færre alvorlige læsioner hos fødende" for et eksempel på en sådan analyse af mulig kausalitet (15).
Kriterierne er:
1: Styrken af associationen – fx udtrykt ved en Odds Ratio eller Relativ Risiko.
2: Konsistens af associationen – virker interventionen andre steder end hvor den indføres?
3: Specificitet af associationen – kan andre samtidige forhold have forårsaget resultatet?
4: Temporaliteten – indtraf en evt. forbedring i resultatet i passende tidsmæssig relation til starten på interventionen?
5: Biologisk gradient – er der en dosis-responsvirkning? Dette er ofte vanskeligt at vise, men kan evt. demonstreres med regressionsanalyse, hvis registreringerne er tilstrækkeligt detaljerede.
6: Sandsynlighed – er der en biologisk rimelighed i at antage, at forholdet mellem intervention og resultat kan være kausalt?
7: Kohærens – kan den evt. fundne association bekræftes af eksisterende viden på feltet?
8: Analogi – er den givne association i overensstemmelse med fx fysiologiske undersøgelser o.l. på området?
9: Eksperiment - kan man ved at manipulere med interventionen se relaterede ændringer i resultatet som forventet?
Case: Projekt Færre alvorlige læsioner hos fødende. Bradford hill kriterierne anvendt til vurdering af mulig kausalitet mellem intervention og resultat
Konklusion er, at Bradford Hill kriterierne støtter en antagelse om et kausalt forhold mellem intervention og det forbedrede resultat. |
Hvilke data er der brug for, når et kvalitetsforbedringsprojekt skal publiceres?
Det kræver en del at skulle beskrive indikatorerne i et kvalitetsforbedringsprojekt (16) (se også hvornår ved vi, at en forandring er en forbedring og SPC for læger). Begrundelsen for, at man typisk ønsker at registrere meget detaljeret er, at det giver mulighed for at analysere interventionen efterfølgende og derved udtale sig om, hvilke af elementerne der var særligt betydningsfulde og måske gav en statistisk signifikant forskel. Samtidig får man mulighed for at analysere populationerne før og efter starten på en intervention for eventuelle ændringer i baggrundsforhold, som kan tænkes at have haft betydning for resultatet.
Resultatindikatorer og ulempeindikatorer
Der er brug for data, som beskriver det resultat, vi ønsker at forbedre for vores patienter – dvs. resultatindikatorerne. I samme kategori er de indikatorer, som beskriver eventuelle ulemper som følge af projektet. Anonyme data kan lettest opsamles i et afkrydsningsskema (et ”ølregnskab” eller ”stakitter”). Derved kommer man hurtigt i gang, men afskærer sig fra efterfølgende validering af data og ikke mindst fra nærmere statistisk analyse, hvilket ikke er tilfredsstillende, hvis man stiler efter at publicere sit arbejde.
I stedet kan disse data ofte hentes fra den elektroniske patientjournal. De fleste vil have brug for hjælp fra en lokal datamanager eller tilsvarende ekspert til at foretage disse udtræk. Det skal godkendes af afdelingsledelsen, før man starter på at samle data over en af afdelingens patientgrupper. Der er ikke aktuelt lovmæssigt krav om godkendelse fra den lokale videnskabsetiske komite eller Datatilsynet, når anonymiserede data samles ind til forbedringsprojekter. Men der er naturligvis krav om, at man opbevarer og håndterer data sikkert og korrekt. Man vil desuden gøre klogt i at tjekke, om listerne fra den elektroniske patientjournal over patienter med de relevante diagnose- eller procedurekoder er korrekte og valide fx ved at gennemgå alle patienter (eller en passende stikprøve) for en passende periode.
Resultatdata vil i princippet kunne hentes fra forskellige fagspecifikke kvalitetsdatabaser, som er tilknyttet RKKP, men specielt hvis der skal arbejdes med og omdefineres på fx den relevante undersøgelsespopulation, vil man som oftest løbe ind i krav om at skulle betale for adgangen fx via Forskerservice i Sundhedsdatastyrelsen. Det er desværre sjældent inden for rammerne af kvalitetsforbedringsprojekter at have adgang til økonomiske ressourcer for at få adgang til data, heller ikke når det er data fra egen afdeling og til gavn for patienterne i egen afdeling.
Vanskelighederne med adgang til data bliver større, hvis man ønsker at hente data ud som tidstro diagrammer fremadrettet og altså ikke kun til brug i et snævert afgrænset projekt. Der er mulighed for, at man lokalt kan løse problemerne ved hjælp fra IT-afdelingen, datamanagere og ikke mindst opbakning fra ledelsen lokalt.
Procesdata
Selve sjælen i et kvalitetsforbedringsprojekt er procesdata (17). Det er disse data, som afslører, om den nye forbedrede proces bliver implementeret eller ej. Hvis den ikke bliver implementeret, kan man ikke forvente nogen forbedring i resultatet. Det er derfor helt centralt at holde løbende øje med disse data. Det kræver tidstro registrering og ikke mindst tidstro udtræk af data med henblik på feedback til projektet og behandlerne. Disse data bliver typisk ikke registreret i forvejen i den elektroniske patientjournaler, og desværre er det sjældent muligt - eller kun med lang latenstid muligt - at oprette denne registrering.
Konsekvensen heraf er uheldigvis, at man som oftest bliver nødt til at registrere procesdata særskilt, hvorved det er besværligt at koble dem til resultatdata. Alternativt kan man foretage registreringen af alle data i en særlig projektdatabase, hvilket kan medføre behov for dobbeltregistrering af data. Den mest stringente måde at håndtere data på er, at man opbevarer data i en særskilt database inden for organisationens firewall i anonymiseret form, mens analyseprogrammet og udtræk med diagrammer holdes adskilt.
Det kræver således en nøjere afvejning, før man bestemmer sig for, hvordan og hvor man skal opsamle data. Uheldigvis vil besværlighederne med data og manglende ressourcer til at kunne tilkøbe sig adgang til data og analysere dem medføre, at mange vil afstå fra at løfte kvalitetsforbedringsarbejdet mere videnskabeligt, så det kan publiceres.
Hvor kan man publicere kvalitetsforbedringsprojekter?
For den som står for at skulle publicere for første gang, vil det være klogt at øve sig i egen afdeling og egen institution med at få erfaringer med at præsentere sit projekt. Start med at lave en udførlig gennemgang af projektet på baggrund af SQUIRE guidelines. Med den ballast gør man det nemmere for sig selv at lave kortere eller mere dybdegående fremstillinger og præsentationer.
Præsentation af et projekt internt i afdelingen i form af opslag og postere for kollegerne og eventuelt også for patienterne er en god start. Det sidste kræver specielt nogle overvejelser ift. måden at præsentere på og naturligvis etiske overvejelser.
Næste trin kan være en poster til møder inden for ens arbejdsområde eller til nationale og internationale kongresser. Fagspecifikke kongresser vil ofte acceptere indsendte forslag til en poster, hvis man følger guidelines for publicering, om end der måske i denne type fora sjældnere er blik for den kliniske betydning og værdi for patienterne, når der er tale om en kendt behandling, der ”blot” bliver implementeret konsekvent i henhold til principperne for kvalitetsforbedring (SQUIRE-guidelines).
Den forståelse vil man nok oftere kunne finde i sammenhænge, som mere specifikt handler om kvalitetsforbedring, hvor man til gengæld vil have vanskeligere ved at sætte den mere fagspecifikke problematik ind i den rigtige sammenhæng. Dette er et dilemma, man også vil kunne støde på i forbindelse med publicering i tidsskrifter. Der er ikke nogen nem løsning ud over tålmodighed, udholdenhed og godt arbejde.
Tidsskrifter
Det vil føre for vidt i denne sammenhæng at komme ind på de fagspecifikke fora og tidsskrifter. Inden for kvalitetsforbedringsverdenen i Danmark og internationalt findes der aktuelt en række fora og tidsskrifter. Den efterfølgende gennemgang er ikke fuldstændig.
Ugeskrift for Læger eller Danish Medical Bulletin (engelsksproget) vil kunne være relevante at skrive til for at komme ud med sine projekter til en større offentlighed. Man skal være opmærksom på, at der også for sygeplejersker og jordemødre og andre faggrupper findes særlige fora og tidsskrifter, som kan være relevante mhp. publicering af artikler eller anden omtale af projekter.
Fagspecifikke - kvalitet
Man kan på internettet finde opdaterede gennemgange af relevante tidsskrifter, fx på Improvement Science Research Network (18).
BMJ Open Quality
Et peer reviewed tidsskrift med open access, hvor man kan søge på alle publikationer fra dette tidsskrift. Som ved andre tidsskrifter med åben adgang koster det desværre en del at publicere. Aktuelt cirka 10.000 - 12.000 kr. De antager artikler som beskriver både små og store projekter inden for kvalitetsforbedring fra hele verden, forudsat at man publicerer i henhold til SQUIRE guidelines.
BMJ Quality & Safety in Healthcare
Formentlig det største tidsskrift inden for kvalitetsforbedring. Publicerer nok primært forskning om kvalitetsforbedring, dvs. det kan være vanskeligt at publicere konkrete kvalitetsforbedringsprojekter med mindre de så at sige opfylder et særligt behov eller på anden vis udmærker sig med beskrivelse af nye metoder eller vinkler på et givet problem.
Andre relevante tidsskrifter
- American Journal of Medical Quality
- Joint Commission Journal of Quality and Patient Safety
- Journal of Healthcare Quality
- Journal of Patient Safety
- International Journal of Quality in Healthcare
- Journal of Nursing Care Quality
Fora inden for kvalitetsforbedring
Dansk Selskab for Patientsikkerhed (PS!)
Et godt sted at holde sig orienteret om hvad der sker inden for området (www.patientsikkerhed.dk). Selskabet har forskellige løbende aktiviteter:
- Arrangør af den årlige patientsikkerhedskonference samt en årlig konference om patientsikkerhed på tværs af sektorer. Desuden forskellige andre relevante nationale møder og webinarer.
- Står for uddannelsen som forbedringsagent samt en uddannelse som vejleder/coach for kvalitetsforbedringsarbejde
Danske Regioner
- Står for forskellige tiltag i de forskellige regioner til uddannelse inden for kvalitetsforbedringsarbejde
- Står for et nationalt e-learningsprogram om kvalitetsforbedringsarbejde (http://forbedringsmodellen.dk). Kurset er gratis, kan tilgås hvis man har en regions-mailadresse.
Institute for Healthcare improvement (IHI)
- Står for uddannelse til Improvement Advisor, hvilket foregår i Boston, USA.
- Udgiver en række white papers, som kan downloades fra deres hjemmeside.
Sammen med BMJ (British Medical Journal) står de for at arrangere den årlige internationale konference International Forum for Quality & Safety in Healthcare, om foråret i Europa og om efteråret i Asien. Der er typisk 3.000 – 3.500 deltagere. Der er en stor poster session med gode muligheder for at få antaget en poster. Det er en inspirerende kongres, hvor der ofte er gode ideer at hente med hjem. Desværre er den temmelig dyr med en pris på godt 10.000, - kr. for tre dage. Der kan være mulighed for få opnå rabat, hvis man kontakter Dansk Selskab for Patientsikkerhed i god tid.
Referencer
- 1. Atul Gawande, Better, 2007.
- Oliver D. Should practical quality improvement have parity of esteem with evidence-based medicine? BMJ 2017;357:j2582
- Rasmussen OB, Yding A, Anhøj J, Andersen CS, Boris J. Reducing the incidence of Obstetric Sphincter Injuries using a hands-on technique: an interventional quality improvement project. BMJ Quality Improvement Reports 2016;5:u217936.w7106
- Hollesen RvB, Johansen RLR, Rørbye C, Munk L, Barker P, Kjaerbye-Thygesen A. Successfully reducing newborn asphyxia in the labour unit in a large academic medical centre: a quality improvement project using statistical process control. BMJ Qual Saf 2017;0:1-10. Doi:10.1136/bmjqs-2017-006599.
- Anhøj J, Hellesøe A-MB. The problem with red, amber, green: the need to avoid distraction by random variation in organizational performance measures. BMJ Qual Saf 2016;0:1-4. Doi:10.1136/bmjqs-2015-004951.
- Vaughn VM, Saint S, Krein SL, Forman JH, Meddings J, Ameling J, Winter S, Townsend W, Chopra V. Characteristics of healthcare organisations struggling to improve quality: results from a systematic review of qualitative studies. BMJ Qual Saf 2018;0:1-11. Doi:10.1136/bmjqs-2017-007573.
- Dixon-Woods M. How to improve healthcare improvement—an essay by Mary Dixon-Woods BMJ 2019; 367 :l5514
- https://www.thisinstitute.cam.ac.uk/about/
- Ogrinc G, Davies L, Goodman D, Batalden P, Davidoff F, Stevens D. SQUIRE 2.0 (Standards for Quality Improvement Reporting Excellence): Revised Publication Guidelines from a Detailed Consensus Process. American Journal of Medical Quality 2015, Vol. 30(6) 543–549.
- http://www.equator-network.org/reporting-guidelines/squire/
(tilgået 10. august 2021) - Berwick DM. The Science of Improvement. JAMA, March 12, 2008; Vol 299(10):1182-1184.
- Frieden TR. Evidence for Health Decision Making – Beyond Randomized, Controlled Trials. N Eng J Med 2017;377:465-75.
- Murray D. What should we do when traditional research fails? Editorial, Anaesthesia 2017;72,1055-1068
- Poots AJ, Reed JE, Woodcock T, Bell D, Goldmann D. How to attribute causality in quality improvement: lessons from epidemiology. BMJ Qual Saf 2017;01-6. DOI:10.1136/bmjqs-2017-006756.
- Rasmussen OB, Yding A, Lauszus F, Andersen CS, Anhøj J, Boris J. Importance of Individual Elements for Perineal Protection in Childbirth: An Interventional, Prospective Trial. Am J Perinatol Rep 2018;8:e289-e294.
- Mayerhofer K, Bodner-Adler B, Bodner K, Rabl M, Kaider A, Wagenbichler P, et al. Traitional care of the perineum during birth. J Reprod Med 2002;47:477-482.
- Shah A. Using data for improvement. BMJ 2019;364:I189 (published 15 February 2019).
- Rasmussen OB. Kvaliteten i kvalitetsmodellen – en midtvejsevaluering. Ugeskr Læger 20. marts 2017;179/6:542-543.
- www.isrn.net/blog/qijournals
SPC for læger
Af Jacob Anhøj, overlæge, Diagnostisk Center, Rigshospitalet
Statistisk proces kontrol, SPC, er en gren af den analytiske statistiske videnskab, som bruges inden for kvalitetsudvikling til at forbedre produkter og tjenesteydelser. Centralt i SPC er forståelse for processers variation over tid og sted. Procesbegrebet skal i denne sammenhæng forstås bredt som noget, der modtager input og leverer et resultat. En proces kan fx være en operation og resultatet et udtryk for i hvor høj grad operationen fx afhjælper patienternes smerter. Af hensyn til den statistiske analyse er det nødvendigt, at resultatet kan udtrykkes i tal. Tal, som på denne måde udtrykker kvalitet, kalder vi for indikatorer.
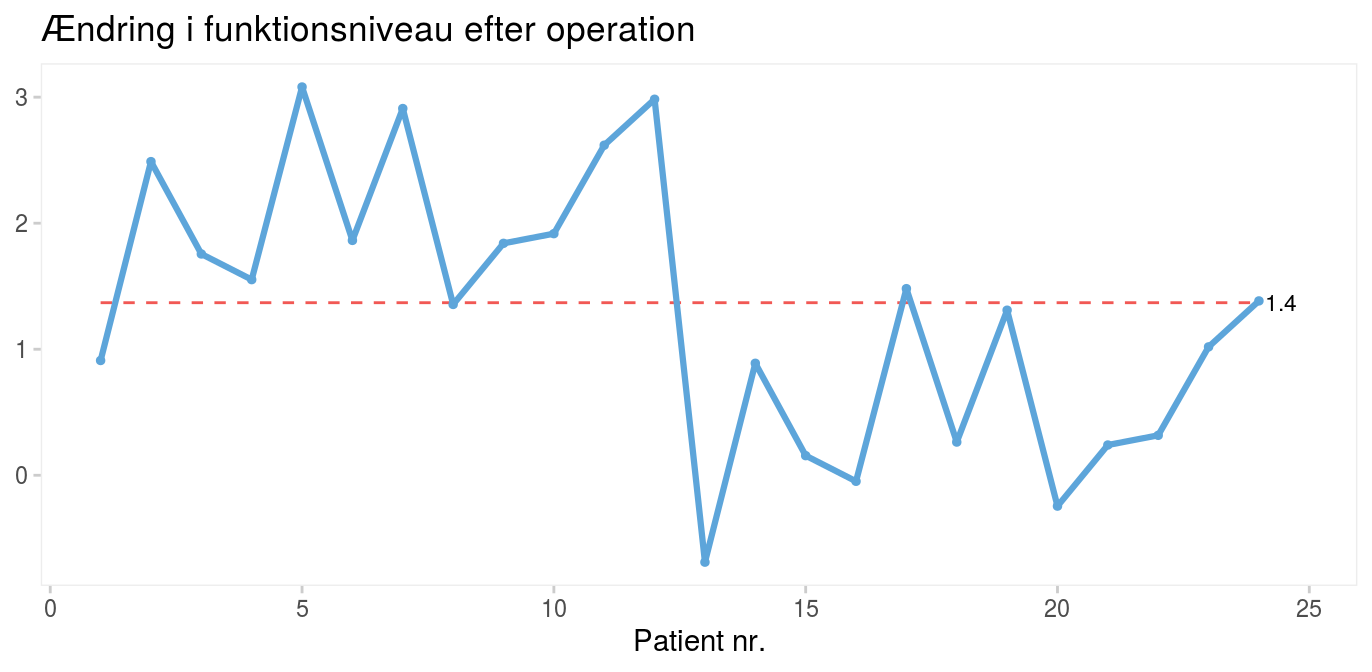
Som et tænkt eksempel kunne vi lade nogle patienter score deres eget behandlingsresultat, fx funktionsniveau, på en visuel analogskala fra -5 til 5, hvor værdier over 0 udtrykker en forbedring, og værdier under 0 udtrykker en forværring.
På grund af variation i utallige faktorer, som har betydning for resultatet, er indikatorværdien sjældent helt ens for to patienter. I nogle tilfælde kan forskelle i behandlingsresultater forklares ved særlige forhold, fx alternativ operationsteknik, konkurrerende sygdomme hos patienten eller defekt udstyr, som bevirkede, at det gik særligt godt eller skidt for en patient. Men i de fleste tilfælde er det ikke muligt entydigt at forklare de forskelle, vi observerer, som andet end naturlig (også kaldet ‘tilfældig’) variation.
|
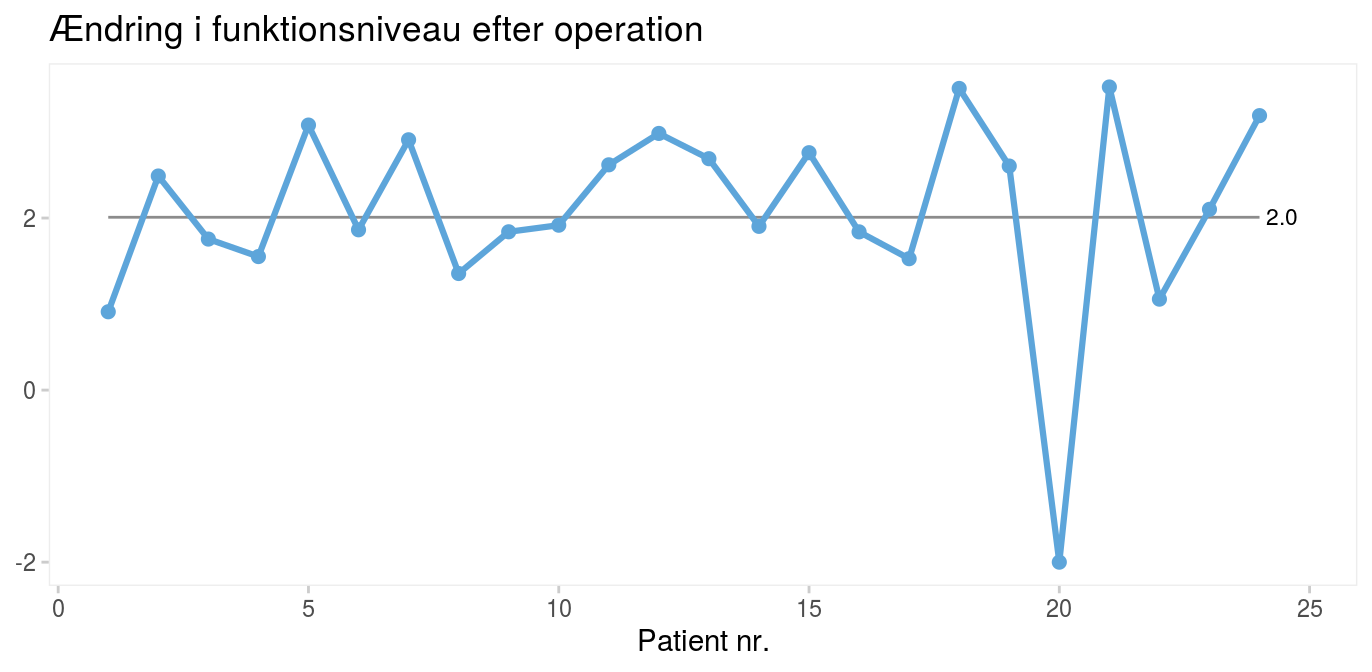
Figur 1: Operationsresultater for 24 fiktive operationer |
Diagrammet i figur 1 viser operationsresultatet fra 24 fiktive operationer. Prikkerne på kurven er afsat i den rækkefølge, patienterne blev opereret. Den vandrette streg markerer den mediane funktionsforbedring, som er 2. Selv om resultatet varierer fra patient til patient, ligger de fleste i nærheden af midtpunktet. Men patient nr. 20 skiller sig ud med en score på -2. En samvittighedsfuld kirurg vil straks spørge “hvorfor?”. Der kan være mange forklaringer, og langt fra alle handler om dårlig operationsteknik. Det væsentlige er at finde årsagen og så vidt muligt forhindre, at det sker igen.
Kvalitetsindikatorer knyttes ofte til kvalitetsstandarder, som udtrykker det ønskede eller forventede niveau for kvaliteten. Standarder kan være enkeltværdier, som udtrykker det lavest eller højest acceptable niveau, eller dobbeltværdier, som udtrykker et ønsket interval for en given indikator (fx INR i et terapeutisk interval).
Det er en vigtig overvejelse, som ofte glemmes, om en standard gælder enkeltmålinger eller aggregerede målinger. Hvis standarden gælder enkeltmålinger, tilstræber vi, at alle målinger ligger på den rigtige side af standarden. Hvis standarden gælder aggregerede målinger, er det tilstrækkeligt, at gennemsnittet eller medianen af alle målingerne ligger rigtigt. Hvis fx standarden for operationsresultatet fastsættes til 1.5, skal vi vide, om den kun er opfyldt, hvis alle patienter scorer over 1,5, eller om det er tilstrækkeligt, at den gennemsnitlige forbedring er over 1,5.
Det er også værd at overveje, om man skal stille krav til variationsbredden – altså, hvor meget må enkeltmålingerne afvige fra hinanden og fra gennemsnittet? De fleste vil nok foretrække så lidt variation som muligt så fx en Big Mac eller en cola smager ens i Hangzhou og i Herning.
God kvalitet betyder derfor to ting: 1: at resultatet varierer mindst muligt og på en forudsigelig måde, og 2: at resultatet lever op til de forventninger, der knyttes til det.
To slags variation
Hovedformålet med at analysere data over tid er at erkende væsentlige ændringer i de underliggende strukturer og processer, som skaber data, så vi kan handle fornuftigt, hvis ændringerne tyder på en forringelse af kvaliteten af vores ydelse.
Men selv om tallene ændrer sig, betyder det ikke nødvendigvis, at den underliggende proces har ændret sig. Og selv når processen ændrer sig, er det ikke altid, at tallene ændrer sig. I eksemplet ovenfor vil de færreste være i tvivl om, at patient nr. 20 repræsenterer en afvigelse. Men ville vi også opfatte det som en afvigelse, hvis patient 20 havde scoret 0? Så hvordan skelner vi mellem tilfældige måleudsving og sikre forandringer?
Walther A. Shewhart, som grundlagde SPC, beskrev to slags variation: almindelig variation (common cause variation) og særlig variation (special cause variation) (Shewhart 1931).
Almindelig variation
- kaldes også tilfældig variation eller støj,
- findes i alle processer,
- skyldes fænomener, som altid er til stede,
- identificerer en stabil og dermed forudsigelig proces.
Særlig variation
- kaldes også ikke-tilfældig variation eller signal,
- findes i nogle men ikke alle processer,
- skyldes fænomener, som ikke normalt er til stede i systemet,
- identificerer en ustabil og dermed uforudsigelig proces.
Evnen til at skelne almindelig og særlig variation fra hinanden er afgørende for valget af forbedringsstrategi. Er processen ustabil (= særlig variation), bør man søge at finde årsagen eller årsagerne til ustabiliteten og eliminere eller implementere disse alt efter, om afvigelserne går den forkerte eller rigtige vej. Målet er at stabilisere processen på det ønskede niveau.
Er processen derimod stabil (= almindelig variation), skal man spørge sig selv, om den er tilfredsstillende: Opfylder den “kundens” (patientens, ledelsens, borgerens, samfundets osv.) behov og forventninger? Hvis det er tilfældet, er det vigtigt at beholde hænderne i lommen og undgå at forstyrre processen, selv om målingerne tilfældigt går op og ned. At reagere på tilfældige udsving kaldes tampering og kan medføre øget variation (Quality America Inc. 2016).
Er processen stabil men utilfredsstillende, er det nødvendigt med gennemgribende forandringer i de underliggende strukturer og arbejdsgange, som driver processen, for at flytte den til det ønskede niveau.
| Stabil proces | Ustabil proces | |
| Tilfredsstillende resultat |
Alt i orden: Kontrollér processen: Overvåg processen, minimér uønsket, tilfældig variation. |
Procesproblemer: Stabilisér processen: Eliminér uønsket eller implementér ønsket ikke-tilfældig variation. |
| Utilfredsstillende resultat |
Produktproblemer: Revidér processen: Optimér strukturer, procedurer og arbejdsgange, så processen flytter sig og stabiliseres på et nyt og bedre niveau. |
Kaos: Stabilisér processen: Eliminér uønsket eller implementér ønsket ikke-tilfældig variation. og Revidér processen: Optimér strukturer, procedurer og arbejdsgange, så processen flytter sig og stabiliseres på et nyt og bedre niveau. |
Tabel 1: Tabellen viser de fire tilstande, som en proces kan befinde sig i, og de tilhørende passende handlinger.
Shewharts kontroldiagram
Shewhart opfandt kontroldiagrammet i 1924 som et enkelt redskab til at skelne mellem almindelig og særlig variation i produktionsprocesser. Shewhart arbejdede på det tidspunkt i inspektionsafdelingen på Bell Labs, som producerede telefonapparater. Han beskrev i sin første bog fra 1931 en lineær og ineffektiv metode til kvalitetskontrol: specifikation → produktion → inspektion. Man inspicerede simpelthen alle færdige produkter og kasserede eller reparerede dem, der ikke overholdt specifikationerne. Shewhart fandt ud af, at man ved at indarbejde kvalitetsstyring i alle led af produktionskæden, kunne minimere eller ligefrem undgå, defekte produkter i sidste ende og dermed spare virksomheden for mange resurser. Det var til dette formål, han opfandt kontroldiagrammet, som gjorde det muligt for medarbejderne ved samlebåndet at vide, hvornår og hvordan (som i tabel 1) de skulle reagere på afvigelser i løbende kvalitetsmålinger i de forskellige led af produktionskæden.
Kontroldiagrammet er et xy-diagram med prikker forbundet med lige streger. X-aksen viser tiden eller rækkefølgen af målingerne, og y-aksen viser indikatorværdierne. En vandret linje markerer datas midtpunkt (som regel gennemsnittet), og grænserne for den almindelige variation vises som en øvre og nedre kontrolgrænse markeret med grå baggrund i figuren.
|
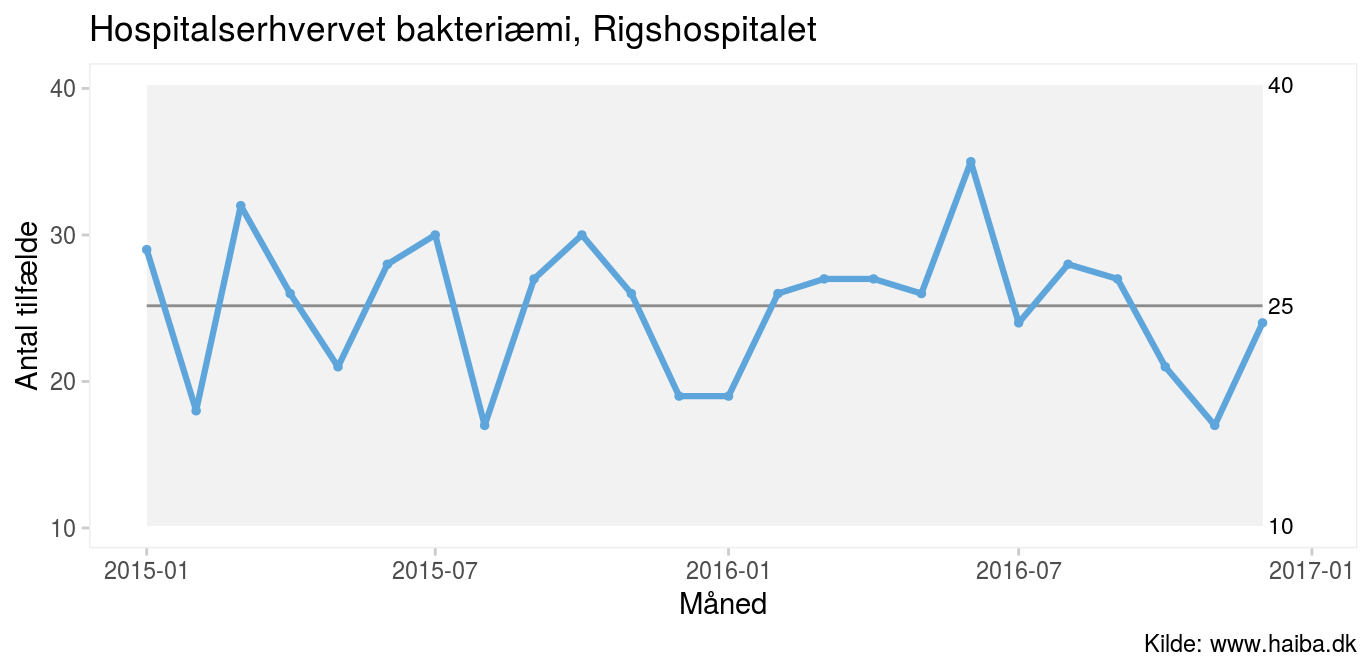
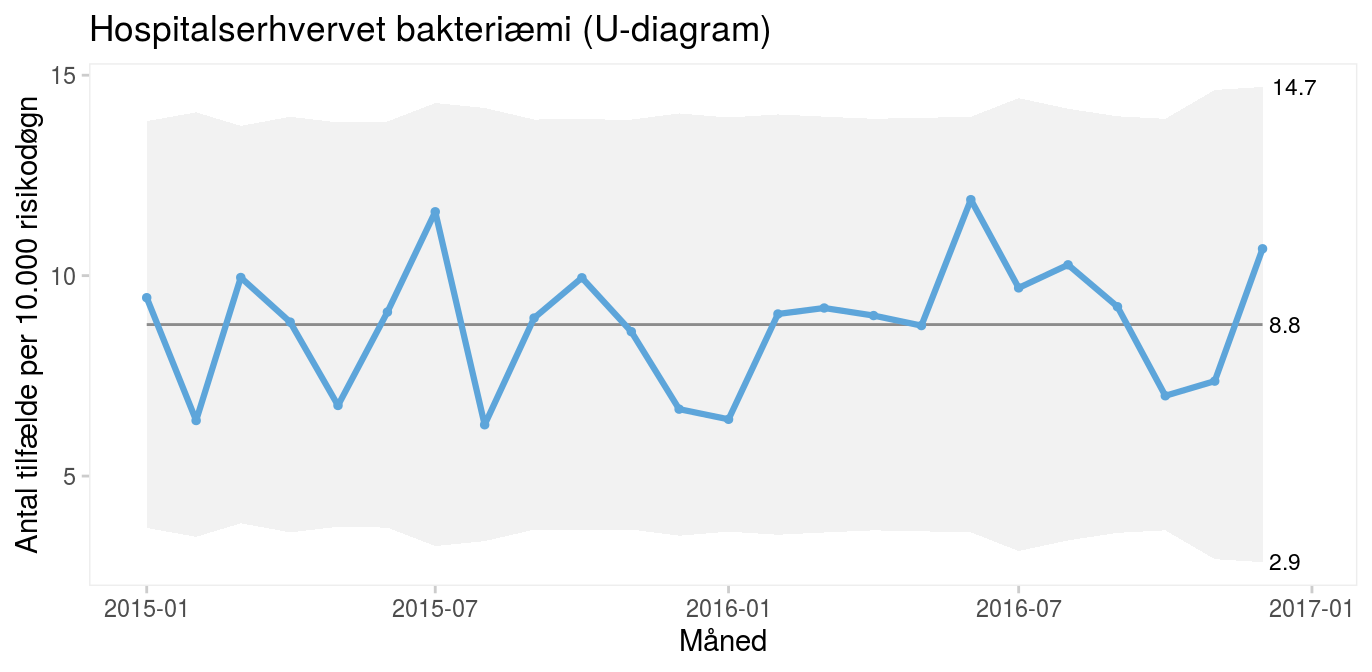
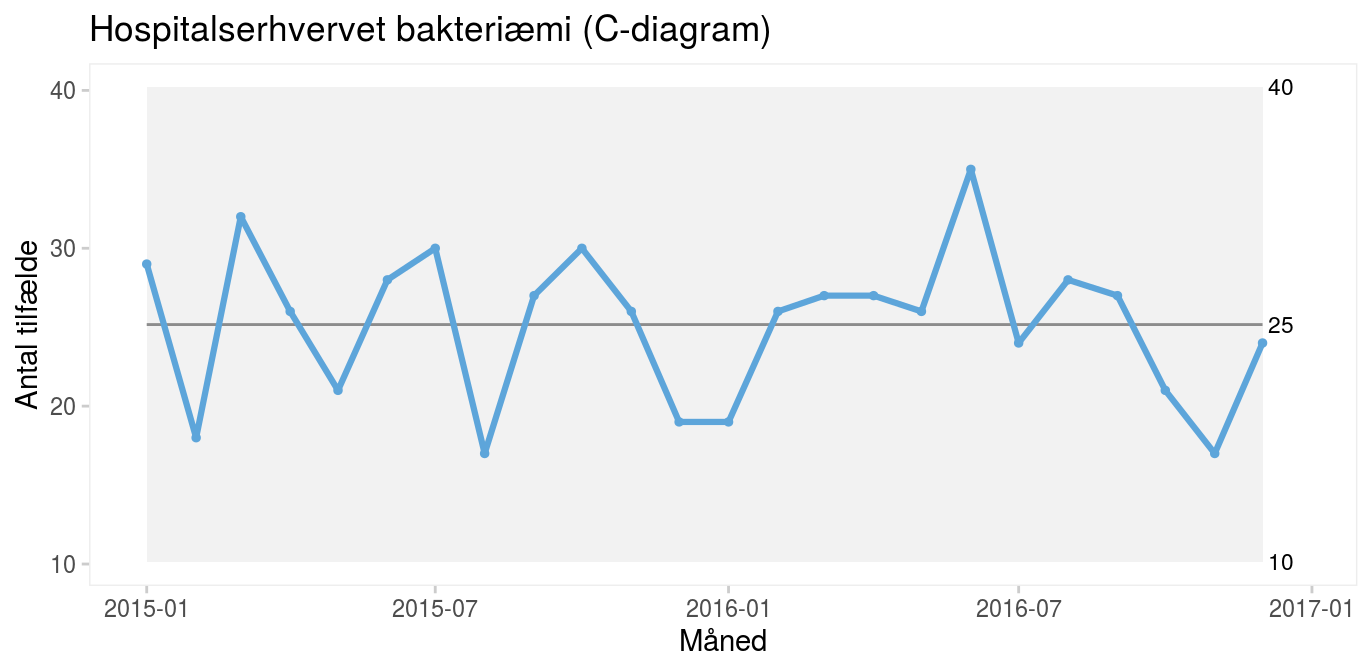
Figur 2: Kontroldiagram visende antal tilfælde af hospitalserhvervet bakteriæmi på Rigshospitalet |
Kontrolgrænserne placeres normalt ved +/- 3 standardafvigelser (SD eller ‘sigma’) fra midtlinjen. I figuren ovenfor er øvre og nedre kontrolgrænse hhv. 10 og 40. Bemærk, at standardafvigelsen, som indgår i beregningen, er den estimerede almindelige variation – ikke den puljede standardafvigelse af alle datapunkterne, som også omfatter eventuel særlig variation. For at undgå misforståelser bruger de fleste betegnelsen sigma om den standardafvigelse, som indgår i beregning af kontrolgrænser.
Udregning af kontrolgrænser forudsætter antagelser om datas teoretiske sandsynlighedsfordeling, og der findes mange forskellige typer kontroldiagrammer til forskellige typer data. Men fortolkningen er enkel og ens for dem alle: Hvis alle målepunkterne ligger mellem kontrolgrænserne, er der almindelig variation. Målepunkter uden for kontrolgrænserne indikerer særlig variation. Vi vender tilbage til beregning af kontrolgrænser i afsnittet om valg af kontroldiagram.
Kontroldiagrammet ovenfor viser den månedlige forekomst af tilfælde af hospitalserhvervet bakteriæmi på Rigshospitalet i perioden 2015-2016. I gennemsnit er der 25 tilfælde om måneden. De fleste måneder er der mellem 20 og 30 tilfælde og enkelte måneder lidt flere eller færre. Kontrolgrænserne viser, at den almindelige variation spænder fra 10 til 40 tilfælde om måneden. Med andre ord: hvis intet forandrer sig, skal vi i fremtiden ikke undre os, hvis der en enkelt måned er så få som 10 eller så mange som 40 tilfælde.
Det er vigtigt at forstå, at kontrolgrænserne beregnes ud fra den naturlige variation, dvs. de fortæller, hvad processen er i stand til at levere, hvad enten vi bryder os om det eller ej. Kontrolgrænser er altså noget ganske andet end specifikationsgrænser og standarder, som taler med kundens stemme dvs., hvilket niveau vi ønsker os. Nogen vil måske mene, at grænserne for den naturlige variation i bakteriæmital er uacceptabelt brede. Men det er der ikke noget at gøre ved, sådan fungerer processen, og hvis man ønsker andre grænser, må man ændre processen.
God kvalitet – som i øverste venstre kvadrant i tabel 1 – er når processen og kunden taler med én stemme, dvs. når processen er stabil, og standarden (dvs. målsætningen) ligger på den rigtige side af midtlinjen eller kontrolgrænserne afhængig af, om den vedrører enkeltmålinger eller aggregerede målinger. Hvis fx Rigshospitalet beslutter, at mere end 35 hospitalserhvervede bakteriæmier på en måned er uacceptabelt, er målet at bringe øvre kontrolgrænse ned under 35 ved at rykke hele processen ned. Hvis standarden derimod gælder gennemsnitsniveauet over længere tid, er alt i orden, fordi gennemsnittet på 25 ligger bekvemt under standarden.
Statistiske test til påvisning af særlig variation
Almindelig variation er karakteriseret ved, at selv om vi ikke kan forudsige den præcise placering af det næste datapunkt, fordeler datapunkterne sig forudsigeligt omkring et givet centrum og inden for visse grænser. Særlig variation betyder, at processen ændrer sig, så vi ikke længere kan forudsige centrum og/eller grænser (før en ny, stabil proces er etableret).
Tag fx en almindelig sekssidet terning. Det er umuligt at forudsige resultatet af det næste kast; men vi ved, at fremtidige kast vil antage værdier mellem 1 og 6, at sandsynligheden for hvert muligt udfald er 1/6, og at gennemsnittet ligger tæt på 3,5. Hvis en terning pludselig viser 7, vil vi undre os. Eller tilsvarende, hvis terningen pludselig viser samme værdi mange gange i træk, ved vi, at der er sket noget usædvanligt, og at det vil kunne betale sig at lede efter årsagen.
Test for særlig variation bygger på påvisning af mønstre i data, som ville være usædvanlige i tilfældige og forudsigelige processer.
Shewharts 3 sigma-regel
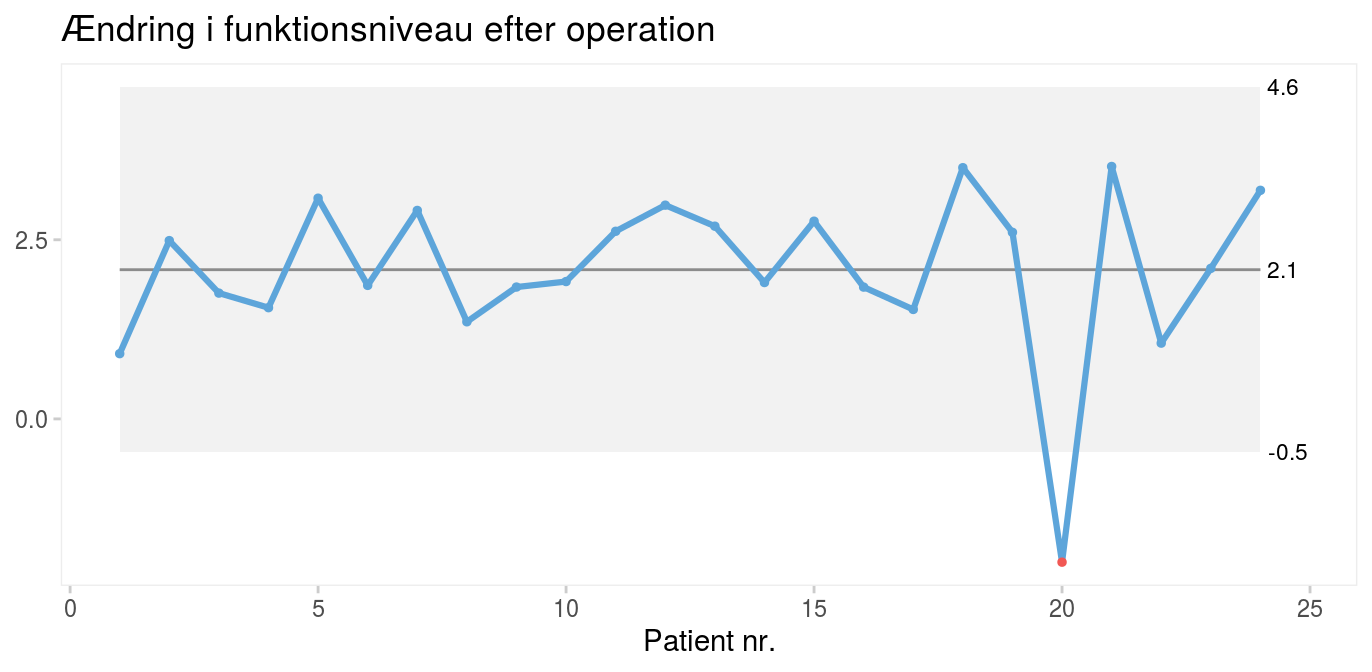
Shewharts oprindelige 3 sigma-regel (et eller flere datapunkter ligger uden for kontrolgrænserne) er effektiv til at opdage større, eventuelt forbigående udsving i processen. Patient nr. 20 fra kirurgieksemplet (figur 3) falder tydeligt uden for nedre 3 sigma-kontrolgrænse og repræsenterer derfor særlig variation.
|
Figur 3:Operationsresultater for 24 fiktive operationer (som i figur 1). |
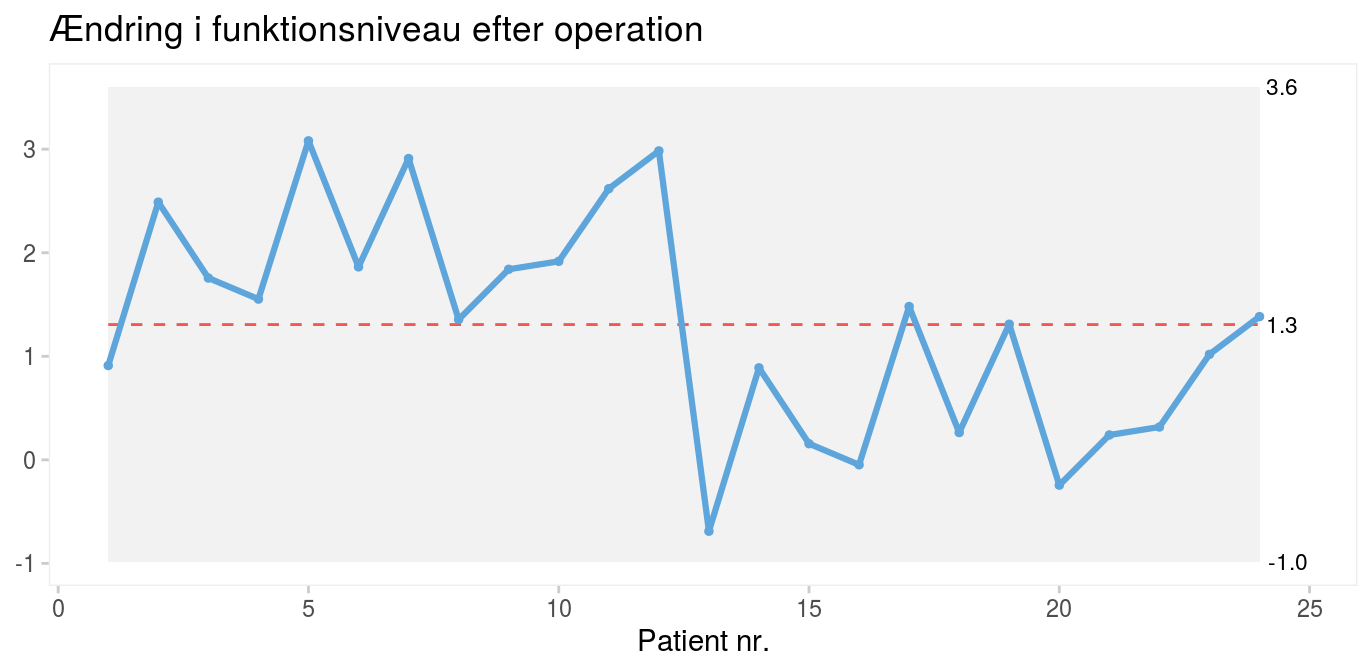
3 sigma-reglen er derimod ikke effektiv til at opdage mindre skift (dvs. ændringer) i processen som i næste tænkte eksempel (figur 4), hvor der tydeligvis sker et skift efter patient nr. 12, selv om alle datapunkterne ligger mellem kontrolgrænserne.
|
Figur 4: Operationsresultater for 24 fiktive operationer (ny patientserie). |
Derfor er der i tidens løb udviklet mange supplerende test til at øge kontroldiagrammers mulighed for at afsløre andre former for skift i kvaliteten end pludselige store udsving.
Western Electric-reglerne
De bedst kendte test for særlig variation er formentlig The Western Electric Rules (WE), som optræder første gang i Statisitical Quality Control Handbook i 1956 (Western Electric Company 1956). WE-reglerne er fire enkle tests, som kan appliceres på kontroldiagrammet alene ved at kigge på det og baserer sig på at findeusædvanlige mønstre i datapunkternes placering i forhold til kontrolgrænserne og midtlinjen.
- Et eller flere datapunkter ligger uden for kontrolgrænserne (Shewharts oprindelige 3 sigma-regel).
- To ud af tre konsekutive datapunkter er mere end 2 sigma fra midtlinjen (to tredjedele af afstanden mellem midtlinje og kontrolgrænsen).
- Fire ud af fem konsekutive datapunkter er mere end 1 sigma fra midtlinjen.
- Otte konsekutive datapunkter ligger på samme side af midtlinjen.
Figur 4 er således positiv for både regel 2, 3 og 4.
WE-reglerne øger kontroldiagrammets følsomhed for mindre, men vedvarende skift i data, og dermed kan det anvendes til at identificere mindre men mere vedvarende ændringer i fx kvaliteten af en ydelse. Reglerne har vist deres værd gennem mere end et halvt århundrede og er standard i mange virksomheder verden over.
Det er værd at bemærke, at WE-reglerne fungerer bedst, når kontroldiagrammet har mellem 20 og 30 datapunkter. Med færre end 20 datapunkter, mister reglerne sensitivitet (flere falsk negative), og med flere end 30 datapunkter mister de specificitet (flere falsk positive).
I Western Electric-håndbogen findes i øvrigt mange flere regler til påvisning af særlige typer af særlig variation. Men det er vigtigt at være opmærksom på, at selv om det kan være fristende at bruge mange tests for at øge følsomheden af sin analyse, stiger risikoen for falske signaler med antallet af test – jo flere regler, man applicerer, jo flere falske signaler skal man være villig til at forholde sig til. Det behøver ikke være et problem, hvis omkostningerne ved årsagsanalyse er beskedne. Men hvis et signal udløser fx produktionsstop eller dyre kerneårsagsanalyser, skal man nøje opveje omkostningerne ved at overse et skift mod omkostningerne ved falske signaler. Beslutningen om, hvor mange og hvilke test, der skal indgå i analysen er derfor vigtig og skal baseres på meget andet end statistiske overvejelser.
Test for lange serier og få kryds
To nyere regler for særlig variation baserer sig alene på datapunkternes placering i forhold til midtlinjen (Anhøj og Olesen 2014; Anhøj 2015):
- Skiftreglen: Usædvanligt lange serier. En serie (run) er et eller flere konsekutive datapunkter på samme side af midtlinjen. Datapunkter, som ligger direkte på midtlinjen hverken bryder eller bidrager til serien. Den øvre 95% prædiktionsgrænse for længste serie er omtrent log2(n)+3 afrundet til nærmeste heltal, hvor nner antallet af brugbare datapunkter (datapunkter som ikke ligger på midtlinjen). Med 24 datapunkter vil en serie på mere end 8 datapunkter indikere særlig variation.
- Krydsreglen: Usædvanligt få kryds. Et kryds er når to nabopunkter ligger på hver sin side af midtlinjen. I en tilfældig proces vil antallet af kryds være binomialfordelt, b(n−1,0.5), hvor n er antallet af brugbare observationer og 0.5 er sandsynligheden for, at et datapunkt befinder sig hhv. over eller under midtlinjen. Den nedre 5% prædiktionsgrænse for antal kryds er den kumulative fordelingsfunktions nedre 5% grænse. Med 24 datapunkter vil færreend 8 kryds indikere særlig variation.
Grænseværdier for længste serie og antal kryds i tilfældige talrækker med 10-100 datapunkter.
Skift- og krydsreglerne er bedre end 3 sigma-reglen og sammenlignelige med WE-regel 2-4 til at påvise moderate men vedvarende skift i data over tid (Anhøj og Wentzel-Larsen 2018). Derudover har de nogle ekstra fordele:
- De er uafhængige af kontrolgrænser og kan derfor bruges alene i såkaldte seriediagrammer, som er enklere at konstruere og ikke forudsætter antagelser om datas teoretiske sandsynlighedsfordeling. Vi ser nærmere på seriediagrammet nedenfor.
- Fordi grænseværdierne for længste serie og antal kryds af midtlinjen afhænger af antallet af datapunkter, holder reglerne nogenlunde konstant sensitivitet og specificitet i diagrammer med så få som 10 og op til uendeligt mange datapunkter.
Serielængde og antal kryds er to sider af samme sag – lange serier giver færre kryds og omvendt – og begge regler, sammen eller hver for sig, indikerer særlig variation. Reglerne kan således opfattes som alternativer til WE-regel 2-4. De kan benyttes sammen med 3 sigma-reglen i kontroldiagrammer eller alene i seriediagrammer.
I det foregående kontroldiagram (figur 4), hvor alle datapunkterne ligger mellem kontrolgrænserne, finder vi særlig variation i form af en lang serie på 11 datapunkter (mod forventet højst 8) og kun 7 kryds (mod forventet mindst 8). Bemærk den røde, stiplede midtlinje, som indikerer ikke-tilfældig variation i form af enten for lange serier eller for få kryds.
Seriediagrammet
Skift- og krydsreglerne kan som sagt bruges alene i seriediagrammer, som ligner kontroldiagrammer, men mangler kontrolgrænser, og hvor midtlinjen som regel er medianen (dvs. Er placeret som en vandret linje svarende til den midterste værdi af datapunkterne). Med seriediagrammer behøver man derfor ikke besvære sig med komplicerede udregninger af kontrolgrænser; og med medianen som centrum behøver man ikke – som med kontroldiagrammer – bekymre sig om datas fordeling, som per definition altid vil være symmetrisk omkring medianen.
Figur 5 viser et seriediagram med samme datasæt som i kontroldiagrammmet i figur 4.
|
Figur 5; Operationsresultater for 24 fiktive operationer (her præsenteret i seriediagram). |
Seriediagrammet er i sagens natur uegnet til at opdage selv store, men forbigående skift, som ellers ville blive fanget af kontrolgrænser. Men på grund af sin enkelthed og mere sikre påvisning af vedvarende skift, er seriediagrammet velegnet som førstevalg. Kontroldiagrammet kan så anvendes i de tilfælde, hvor seriediagrammet viser almindelig variation, og hvor det er vigtigt at udelukke større forbigående skift i processen. Hvis seriediagrammet finder særlig variation, er der ingen grund til at beregne kontrolgrænser. Ligesom der sjældent er grund til CT-scanning, hvis diagnosen kan stilles sikkert med en almindelig røntgenundersøgelse.
Serie- og/eller kontroldiagrammer – hvad skal du vælge?
I kvalitetsudviklingslitteraturen får man let det indtryk, at kontroldiagrammer er finere eller bedre end seriediagrammer, hvis eneste fordel er, at de er enkle at konstruere. Det passer bare ikke. Serie- og kontroldiagrammer er forskellige diagnostiske metoder, som komplementerer hinanden. Derfor benytter vi fællesbetegnelsen SPC-diagrammer. Beslutning om, hvorvidt midtlinjen skal være medianen (som i seriediagrammet) eller gennemsnittet (som i kontroldiagrammet), om man skal bruge kontrolgrænser eller ej, og hvilke test der skal udføres, afhænger ikke af hvilket diagram, der er lettest at konstruere, men af analysens formål.
Til kvalitetsudvikling, hvor målet er at flytte en proces fra et niveau til et andet og bedre niveau (og ikke bare at overvåge kvaliteten), og hvor vi derfor forventer særlig variation, kan man med fordel applicere skift og kryds-reglerne i forhold til medianen. Hvis skift og kryds-reglerne signalerer, kan vi med stor sikkerhed sige, at processen har flyttet sig mere end bare forbigående.
Til kvalitetskontrol, når målet er at fastholde en tilfredsstillende proces på et godt og stabilt niveau, og hvor vi forventer almindelig variation, kan man med fordel benytte gennemsnittet som midtlinje og supplere med kontrolgrænser, som er hurtigere til at opdage større udsving i data.
I praksis kan man vælge følgende strategi:
- Beslut målsætning og vælg indikatorer.
- Definer indikatorerne (mere om dette i afsnittet om indikatorer).
- Indsaml data og begynd seriediagram. Dette kan gøres enkelte fx ved hjælp af papir og blyant.
- Efter mindst 12 datapunkter, test for særlig variation i form af usædvanligt lange serier eller usædvanligt få kryds:
- almindelig variation: fastholde eller forbedre?
- særlig variation: eliminere eller implementere?
- Forbedring er opnået og fastholdt, når de seneste mindst 12 målepunkter varierer tilfældigt omkring et nyt og bedre centrum.
- Overvej at anvende et kontroldiagram til at overvåge, stabilisere og fastholde processen.
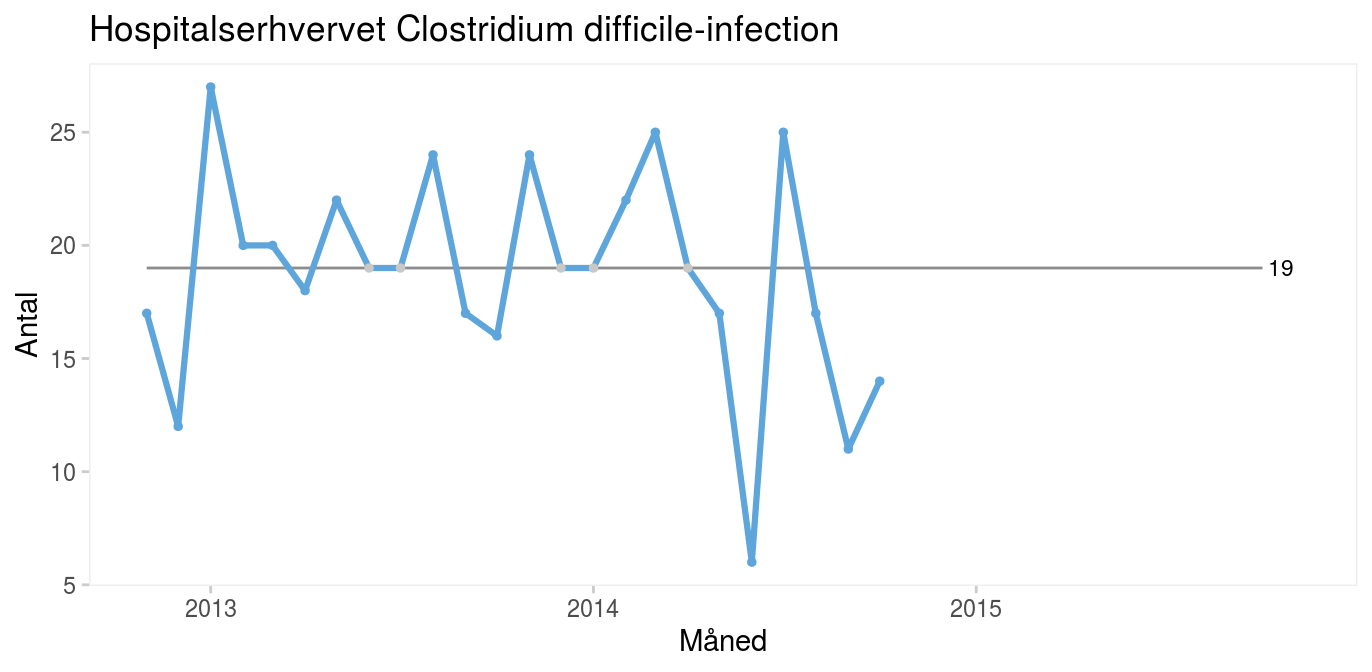
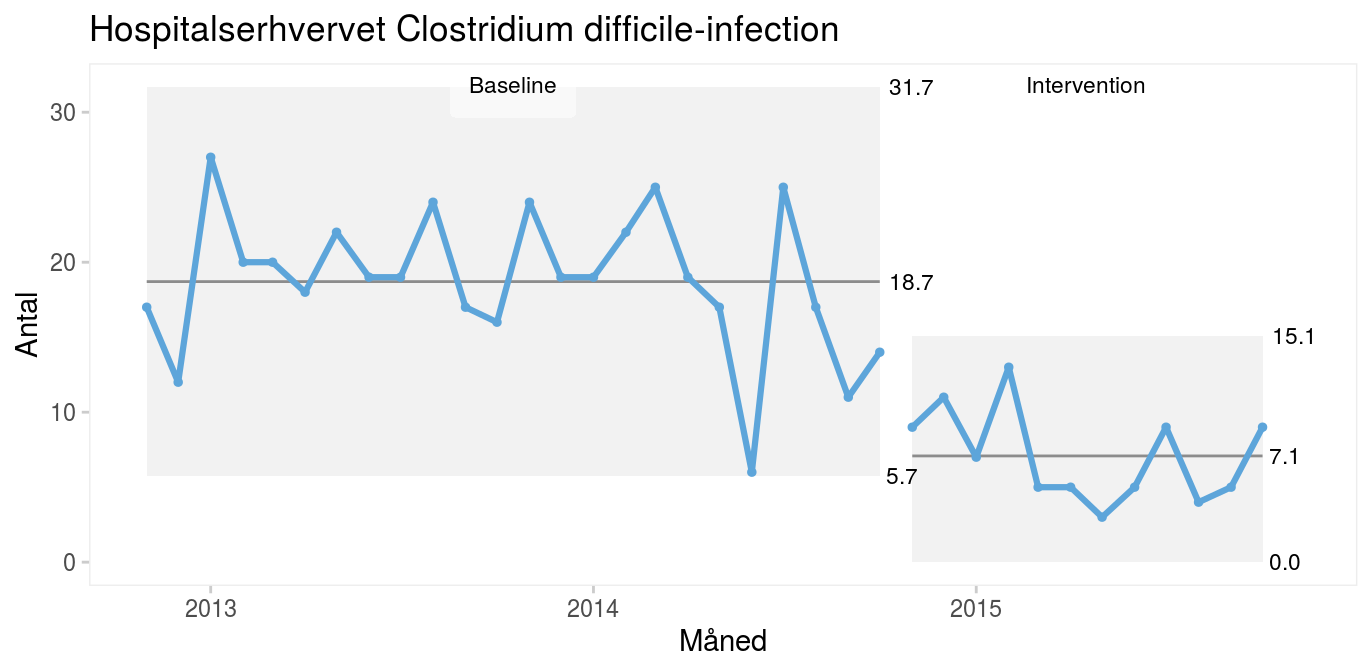
Case: Forebyggelse af Clostridium difficile-infektioner hos indlagte patienterPå Amager-Hvidovre Hospital besluttede man i efteråret 2014 på udvalgte afdelinger at afprøve profylaktisk anvendelse af gærsvampen Saccharomyces boulardii (fås i kapselform i helsekostbutikker) mod Clostridium difficile-infektion hos patienter i antibiotisk behandling (Carstensen m.fl. 2018). Interventionen er velbeskrevet, så formålet var ikke at bevise effekten, men at implementere en ny praksis og reducere risikoen for hospitalserhvervet C. difficile-infektion. Seriediagrammet viser det månedlige antal C. difficile-infektioner på hele hospitalet 24 måneder inden iværksættelse af interventionen (baseline).
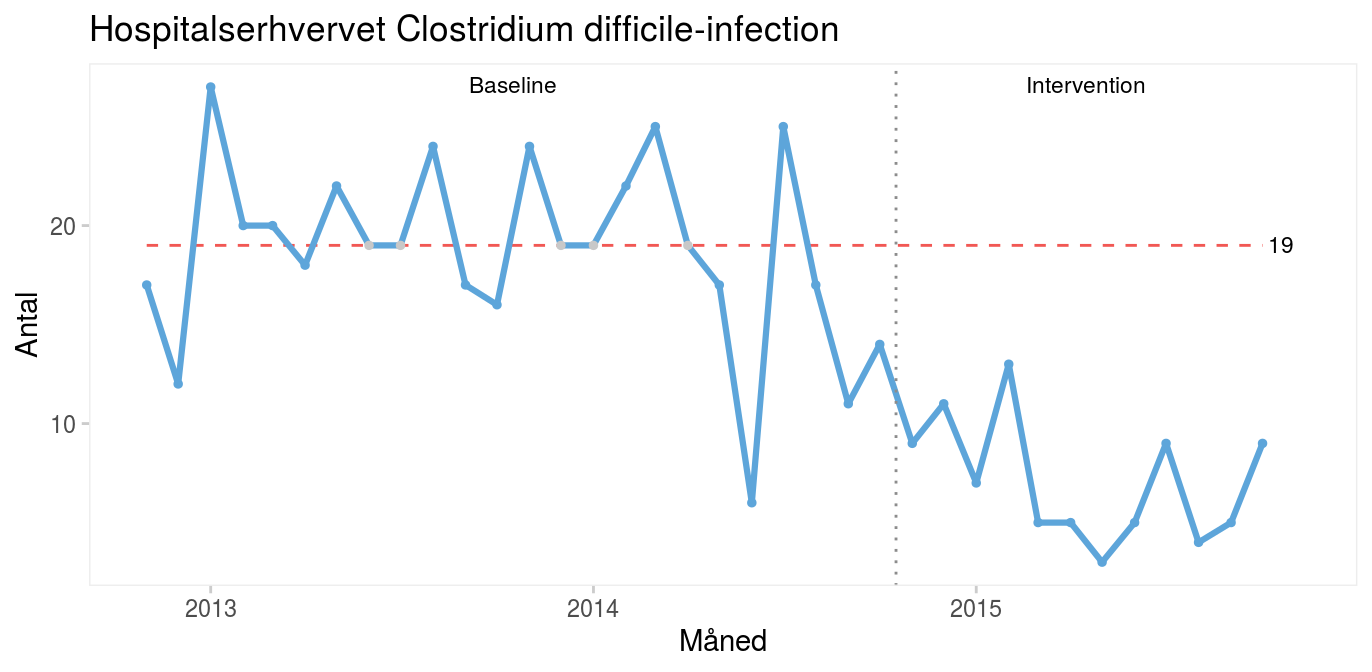
Interventionen begyndte i oktober 2014, og det er tydeligt, at der efterfølgende sker et skift i processen mod færre infektioner. Skiftet signaleres af både en usædvanlig lang serie (15 > 8) og usædvanligt få kryds (8 < 11).
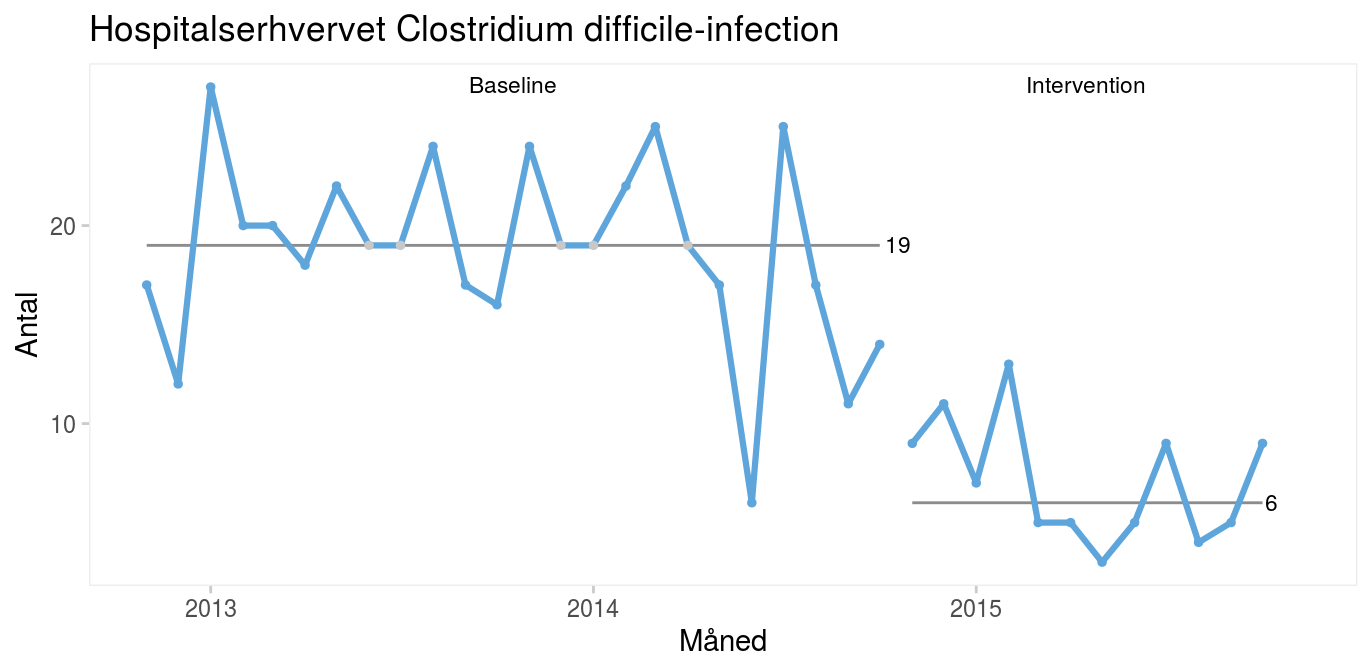
Når processen skifter i den ønskede retning som resultat af en bevidst indsats, kan det være meningsfuldt at opdele diagrammet i to perioder før og efter interventionen.
Fordi begge perioder kun indeholder almindelig variation, kan det være nyttigt at benytte et kontroldiagram til at vise den nye proces’ naturlige grænser.
Kontroldiagrammet viser, at infektionsraten er faldet fra i gennemsnit 19 til 7 tilfælde om måneden efter interventionen, at den nye proces er stabil og dermed forudsigelig, og at vi i fremtiden kan forvente mellem 0 og 15 tilfælde om måneden. Selv om det er meget fristende at konkludere, at interventionen har medført en forbedring, kan man ikke sige det med sikkerhed. Alt, vi ved, er, at forekomsten af C. difficile-infektioner er faldet, efter at vi ændrede praksis. Hvis vi ønsker at bevise en kausal sammenhæng mellem en intervention og et resultat, må vi på anden vis føre bevis for sammenhængen, fx ved at lave et godt gammeldags kontrolleret, randomiseret forsøg eller ved at inddrage Bradford Hills kriterier i argumentationen (se kapitel 14 om publicering). Formålet med løbende kvalitetsudvikling er ikke at bevise årsagssammenhænge men at forbedre kvaliteten. Det gør vi i dette tilfælde ved at implementere kendt viden i form af S. boulardii til forebyggelse af C. difficile-infektioner. |
Valg af kontroldiagram
Der er udviklet mange forskellige typer kontroldiagrammer til forskellige datatyper. Forskellen ligger i måden, kontrolgrænserne skal beregnes på og afhænger bl.a. af, om data er måle- eller tælledata (se afsnit om måle- og tælledata). Tabellen viser de mest benyttede kontroldiagrammer til gængse datatyper; men der er mange flere til særlige formål, og det anbefales, at man konsulterer speciallitteraturen (fx Montgomery 2009), hvis man for alvor skal have gavn af kontroldiagrammer. I næste afsnit om indikatorer findes en nærmere beskrivelse af datatyper.
 |
Tabel 2: viser karakteristika for forskellige typer af diagrammer
Begreberne defekte og defekter er statistiker-jargon for det, man tæller. Man taler om defekte enheder, når man tæller genstande, individer, processer osv., som besidder eller ikke besidder en bestemt egenskab, der som oftest – men ikke nødvendigvis – er uønsket.
En defekt enhed kan fx være en patient med tryksår (et eller flere), en operation som gik galt eller et lokale, som er utilfredsstillende rengjort. Defekte er altså et enten-eller-begreb og opfører sig i naturen ofte tilnærmelsesvist binomialfordelt.
Når man tæller defekter, tæller man fænomener, som er tilfældigt fordelt i tid og rum. En defekt kan fx være et tryksår, en hospitalsinfektion, en plet på gulvet eller et stjerneskud. Defekter opfører sig ofte tilnærmelsesvist poissonfordelt.
Det er vigtigt at vælge det rigtige kontroldiagram til sine data. SPC-software er ukritisk og vil fremstille det diagram, man beder om, uanset om det er passende eller ej. I nogle tilfælde får man nogenlunde samme resultat med forskellige kontroldiagrammer; men ofte får man misvisende kontrolgrænser, hvis ikke diagramtypen passer til data.
Er man i tvivl om valget af kontroldiagram, eller skal man bare have et par hurtige, “håndlavede” kontrolgrænser på sit seriediagram, kan man (næsten) altid benytte I-diagrammet, som er kontroldiagrammernes “schweizerkniv”. I-diagrammet baserer sine kontrolgrænser på den faktiske variation mellem nabomålepunkter og kan i praksis benyttes til de fleste typer data, hvis blot udfaldsrummet (nævneren) er nogenlunde konstant. Først beregner man gennemsnittet (= midtlinjen) af de individuelle datapunkter. Dernæst ganger man den gennemsnitlige absolutte forskel mellem nabomålinger med den statistiske konstant 2,66. Så beregner man kontrolgrænserne ved hhv. at lægge dette tal til og trække det fra gennemsnittet.
Bakteriæmitallene fra før er: 29, 18, 32, 26, 21, 28, 30, 17, 27, 30, 26, 19, 19, 26, 27, 27, 26, 35, 24, 28, 27, 21, 17, 24. Gennemsnittet er 25.2, og den gennemsnitlige absolutte parvise forskel er 5.78. I-diagrammets kontrolgrænser er derfor 25.2 ± 2,66 x 5.78 = 9.8 – 40.6.
Indikatorer
En indikator er som nævnt et tal, som er udtryk for kvaliteten af et produkt eller en tjenesteydelse, og som kan gøres til genstand for statistisk analyse. Traditionelt opdeler man indikatorer i struktur-, proces- og resultatindikatorer.
Strukturindikatorer knytter sig til fysiske og organisatoriske rammer, fx: findes der en brandindstruks? (ja/nej), hvor mange kvadratmeter er der per sengeplads? (decimaltal), eller hvor mange håndvaske findes på afdelingen? (antal). Strukturindikatorer er i sagens natur ofte relativt statiske og bliver derfor sjældent brugt direkte til løbende kvalitetsudvikling. Men strukturindikatorer kan være nyttige til at forstå rammerne og mulighederne for fremtidig kvalitetsudvikling.
Procesindikatorer knytter sig til rutiner og arbejdsgange, fx: ved hvor stor en andel af operationerne har vi gennemført sikker kirurgi-tjeklisten? (procent), eller hvad er den mediane tid fra udskrivelse til afsendelse af epikrise? (tid). Procesindikatorer er kvalitetsudviklerens vigtigste arbejdsredskab, fordi de siger noget om den adfærd, som i sidste ende har betydning for slutresultatet.
Resultatindikatorer knytter sig til kvaliteten set med kundens øjne, fx: hvor mange hospitalsinfektioner har vi? (antal), hvad er overlevelsen efter operation? (procent), eller i hvilken grad hjælper behandlingen? (decimaltal på VAS-skala eller udsagn på Likert-skala). For kunden er resultatindikatorer naturligvis det mest interessante. Men for kvalitetsudvikleren er resultatet blot det naturlige produkt af strukturer og processer. Resultatet bliver ikke bedre af at blive målt, men af grundlæggende forandringer i strukturer og processer.
Endelig er der ulempeindikatorer, som i sig selv kan være resultat- eller procesindikatorer. Man bruger ulempeindikatorer til at opdage eventuelle utilsigtede bivirkninger af de forandringer, man indfører. Det kunne fx være genindlæggelser efter indførsel af accelererede patientforløb. Det hjælper jo ikke, at man reducerer indlæggelsestiden, hvis det medfører, at patienterne kommer igen med komplikationer på et senere tidspunkt. Dette kan ulempeindikatoren være med til at følge.
Afhængig af deres formål kan nogle indikatorer optræde som både den ene og den anden type. I et projekt om forebyggelse af medicinrelaterede genindlæggelser, kan ‘andel epikriser sendt inden to hverdage’ opfattes som en procesindikator, fordi afsendelse af epikriser skal medvirke til at nå målet. Men den vil kunne opfattes som en resultatindikator, hvis projektets formål er forøgelse af andel epikrier sendt inden for to hverdage.
Måletal og tælletal
Som det fremgår af eksemplerne ovenfor, findes indikatorer i mange former med det til fælles, at de kan udtrykkes i tal. Indikatorens talformat har betydning for, hvordan den skal opgøres og præsenteres i fx kontroldiagrammer. Grundlæggende skelner man mellem måle- og tælletal.
Måletal kendes ved at kunne udtrykkes på en kontinuert skala, som i princippet strækker sig fra −∞ til ∞, og hvor værdierne kan have uendeligt mange decimaler. I praksis har mange måletal dog naturlige grænser. Fx kan fysiologiske værdier som højde, vægt, puls, blodtryk osv. i sagens natur ikke være negative.
I produktionsindustrien benytter man i vid udstrækning måletal til kvalitetsudvikling og -kontrol. Fysiske produkter som skruer, bolte og bordplader forventes at leve op til præcise standarder for mål og vægt. Til disse formål vil man derfor bruge kontroldiagrammer til måletal: Et I-diagram, hvis det enkelte målepunkt stammer fra en enkelt måling, eller et Xbar-diagram, hvis et målepunkt er gennemsnittet af flere målinger taget på samme tid eller fra samme stikprøve.
I sundhedsvæsenet er måletal relativt sjældne i forbindelse med kvalitetsudvikling, fordi sundhedskvalitet oftest handler om antal og andele, som er tælletal. Undtagelserne er tid, fx tid til afsendelse af epikrise, og fysiologiske parametre hos enkeltpersoner, fx alder, vægt, blodtryk peak flow, blodsukker, INR osv.
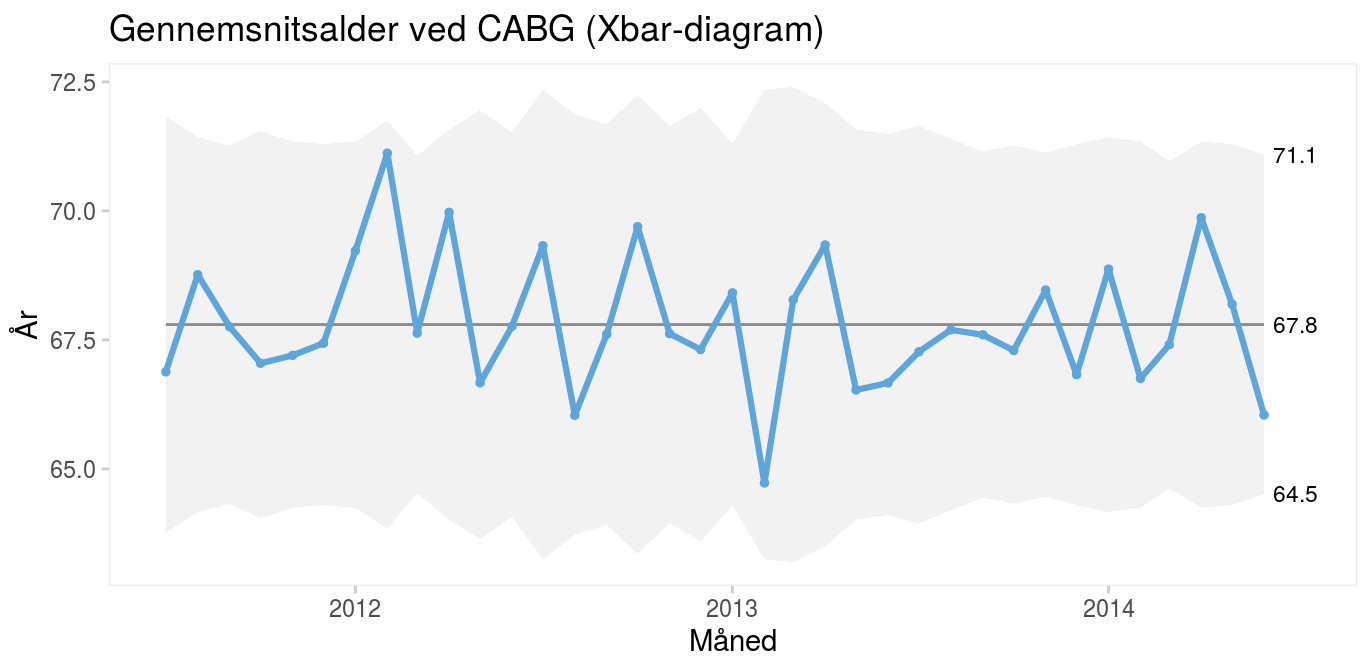
Diagrammet i figur 6 viser gennemsnitsalderen hos patienter, som får foretaget koronar bypassoperation.
|
Figur 6: Gennemsnitsalderen hos patienter, som får foretaget koronar bypassoperation. |
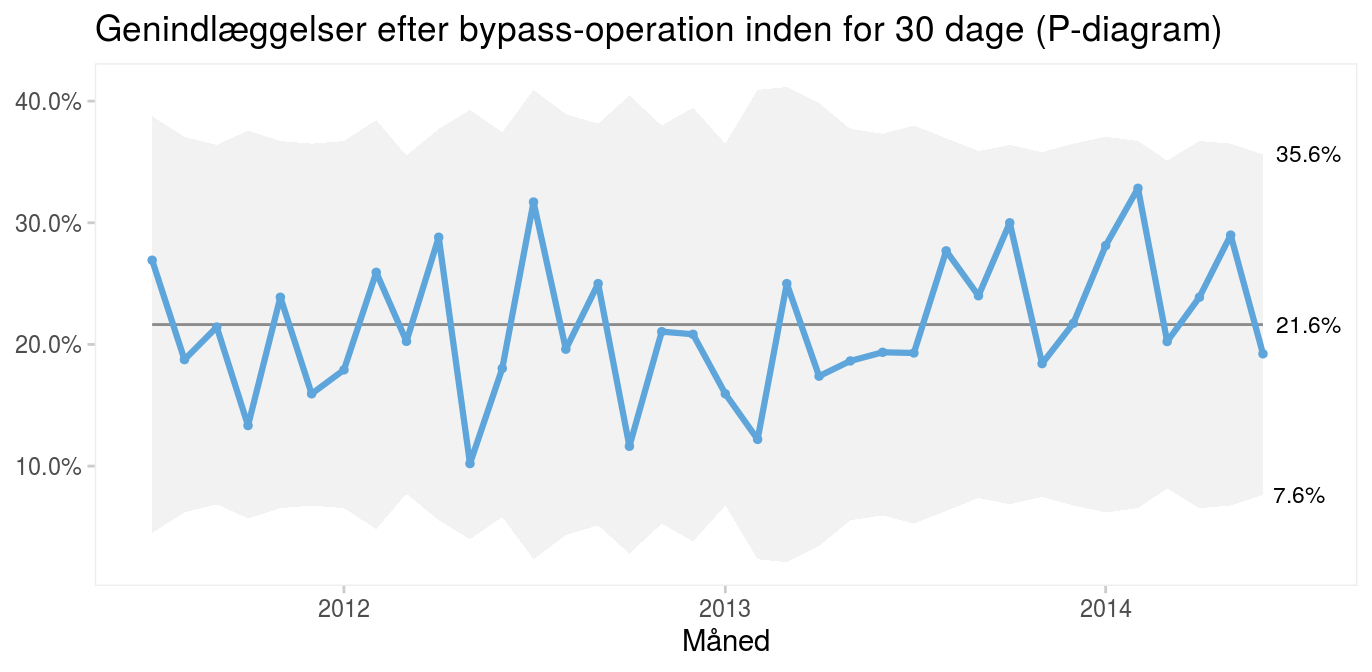
Kontrolgrænserne varierer fra måned til måned fordi, nævneren (antal operationer) varierer. På den måde tager diagrammet højde for naturlige udsving i den almindelige variation, når nævneren varierer. Det samme gælder P- og U-diagrammer.
Tælletal opstår, når man tæller enten individer med bestemte egenskaber (defekte) eller forekomsten af bestemte fænomener (defekter). Tryksår er et eksempel på et fænomen, der kan tælles som både defekte og defekter: antal patienter med tryksår eller antal tryksår. Tæller man antal patienter med tryksår, tæller en patient kun én gang uanset, hvor mange tryksår vedkommende har. Tæller man antal tryksår, tæller hvert tryksår for sig. I begge tilfælde kan man vælge at udtrykke tallet i relation til noget andet, udfaldsrummet, som så indgår som nævner i brøken. Patienter med tryksår kan fx udtrykkes som andelen af patienter med tryksår, og tryksår kan fx udtrykkes som antallet af nyopståede tryksår per 1000 sengedage. Det første tal er en proportion (andel, procent), det andet tal er en rate. Man kender forskel på proportioner og rater ved, at proportioner altid har samme enhed i tæller og nævner (antal patienter med tryksår/antal patienter i alt), og at tælleren ikke kan være større end nævneren, mens rater har forskellige enheder i tæller og nævner (antal tryksår/antal sengedage).
Det er vigtigt at kende forskel på proportioner og rater, når man skal vælge kontroldiagram. Proportioner analyseres med P-diagrammer (P for proportion eller procent). P-diagrammet i figur 7 viser procentdelen af opererede patienter, som genindlægges inden for 30 dage efter operation.
|
Figur 7: P-diagram over procentdelen af genindlæggelser efter bypass |
Rater analyseres med U-diagrammer (U for unequal area of opportunity).
|
Figur 8: U-diagram over antal tilfælde af hospitalserhvervet bakteriæmi. |
Hvis ratens udfaldsrum (area of opportunity) er nogenlunde konstant fra måling til måling, fx antal risikodøgn fra måned til måned som i diagrammet ovenfor, kan man udelade nævneren og benytte et C-diagram (C for count). Fordi C-diagrammer viser et antal frem for en rate, kan de være lettere at forholde sig til end U-diagrammer. Således vil de fleste nok finde det lettere at forholde sig til 25 bakteriæmier om måneden end 8,8 bakteriæmier per 10.000 risikodøgn.
|
Figur 9: C-diagram over antal tilfælde af hospitalserhvervet bakteriæmi. |
Bemærk i øvrigt, at C-diagrammet (figur 9) har samme gennemsnit og kontrolgrænser (efter afrunding) som I-diagrammet (figur 2 – om bakteriæmi i afsnittet om Shewharts kontroldiagram) med de samme data, vi tidligere beregnede “i hånden”.
Stramme indikatorer
Kvalitetsudviklerens vigtigste råstof er gode indikatorer, som kommer af gode data og gode indikatordefinitioner.
Der kan siges og skrives meget om “gode data”. Om de er gode, afhænger i virkeligheden af, hvad data skal bruges til. Ønsker vi bare at vide, om vi har elimineret tryksår eller ej, skal vi blot registrere det første tryksår, der opstår. Men hvis vi fx vil vide, om risikoen for tryksår på vores afdeling er signifikant højere eller lavere end på en tilsvarende naboafdeling, skal vi indsamle data for langt flere patienter med og uden tryksår over lang tid, og vi skal være helt sikre på, at vi tæller tryksår på samme måde hele tiden og på samme måde, som de gør på den afdeling, man sammenligne sig med.
Kort sagt: gode data er data, som er gode nok til formålet.
Gode indikatordefinitioner kan man derimod ikke snakke sig fra. En indikatordefinition er en klar og utvetydig opskrift på, hvordan man omsætter grunddata til en STRAM indikator:
- Sensitiv: indikatoren er følsom for de forandringer, man ønsker at indføre eller undgå.
- Troværdig: indikatoren giver et reelt billede af den kvalitet, man ønsker at måle.
- Reproducerbar: man når frem til de samme tal og konklusioner, når man gentager analysen på de samme grunddata.
- Aktuel: indikatoren viser, hvordan kvaliteten er her og nu – ikke sidste år eller på naboafdelingen.
- Meningsfuld: indikatoren giver mening for brugerne.
De færreste indikatorer er det hele. Tag fx den nu hedengange nationale indikator for hospitalsstandardiseret mortalitetsrate, HSMR. HSMR udtrykker forholdet mellem den faktiske dødelighed og den forventede dødelighed på et hospital, hvor der er taget højde for patientsammensætningen (alder, køn, diagnoser, komorbiditet osv.). HSMR er både meningsfuld, aktuel og reproducerbar. Men den er også – viste det sig – meget lidt sensitiv for reelle kvalitetsforbedringer og -forværringer på hospitalerne. Til gengæld er den følsom for meget andet, fx ændringer i lokal registreringspraksis.
Et andet eksempel er overholdelse af udredningsretten. Indikatoren angiver, hvor stor en andel af patienterne, som har en diagnose eller en plan inden for en fastsat tidsramme. Den er sensitiv, aktuel, reproducerbar og troværdig. Men, fordi den stiller alle symptomer og fund lige, er den i mange tilfælde meningsløs for både klinikere og befolkning.
Et eksempel på indikatorer, som er mindre troværdige, fordi de ikke måler præcis det, man ønsker at måle, men alligevel er nyttige, er forekomsten af hospitalserhvervede infektioner. Hospitalsinfektioner er infektioner, som opstår efter hospitalskontakt (typisk mindst 48 timer efter indlæggelse). I opgørelsen af hospitalsinfektioner indgår oplysninger om patient, indlæggelsestidspunkt og tidspunkt for påvisning af infektion, fx fund af bakterier i urin eller blod. Det giver sig selv, at indikatoren ikke er særligt præcis. Nogle patienter indlægges med infektioner, som først påvises efter et par dage og derfor fejlagtigt tælles med (falsk positive); og andre patienter får en hospitalsinfektion allerede i løbet af de første indlæggelsesdøgn og tælles derfor ikke med (falsk negative). Indikatoren kan altså ikke bruges til at fortælle præcis, hvor mange hospitalsinfektioner der reelt forekommer. Men fordi unøjagtighederne er jævnt og tilfældigt fordelt, kan skift i indikatorniveauet over tid alligevel tages som udtryk for forandringer, som i det mindste bør undersøges nærmere.
Arbejdet med at udvikle gode indikatordefinitioner, som giver STRAMme indikatorer, kan erfaringsmæssigt være noget af det mest tidskrævende og vanskelige inden for klinisk kvalitetsudvikling. Men det skal ikke afholde en fra at gå i gang. Og så skal man huske, at det inden for kvalitetsudvikling er tilladt – ja, endda ønskværdigt – at forbedre sine definitioner undervejs, efterhånden som man bliver klogere.
Der er skrevet tykke bøger om indikatorer; men det væsentlige er, at man har en struktureret tilgang til indikatordefinition, så man ‘når hele vejen rundt om’ indikatoren, inden man går i gang med at samle data
Her er et eksempel på definition af en procesindikator til overvågning af andelen af pneumonipatienter, som har modtaget første dosis antibiotika inden for fire timer efter ankomst.
- Indikatornavn: Rettidig diagnostik og behandling af samfundserhvervet pneumoni.
- Type: Procesindikator.
- Formål: At reducere dødeligheden hos indlagte med samfundserhvervet pneumoni.
- Tællerdefinition: Antal pneumonipatienter, som har modtaget første dosis antibiotika inden for fire timer efter ankomst.
- Nævnerdefinition: Antal pneumonipatienter.
- Datakilde: Morgenkonference.
- Dataindsamling og -behandling: Ved morgenkonferencen noteres (for hver nyindlagt patient med samfundserhvervet pneumoni i det forudgående døgn) dato og tidspunkt for indlæggelse og for første dosis antibiotika. Rådata noteres i et regneark, som automatisk udregner differencen i timer mellem ankomst og behandlingsstart og derefter udregner den ugentlige andel af patienter, hvor antibiotikabehandling er påbegyndt rettidigt.
- Opgørelsesperiode: Ugentligt.
- Analyse og præsentation: Seriediagram.
Særligt punktet om dataindsamling og -behandling kræver afprøvninger og omhyggelighed, så arbejdet med at indsamle data ikke kommer til at overskygge selve forbedringsindsatsen. I praksis kan man med fordel angribe dataindsamlingsdelen som et lille selvstændigt udviklingsprojekt efter alle kunstens regler med formulering af målsætning og iterativ afprøvning af ideer efter PDSA-metoden.
Det er også vigtigt at være omhyggelig med formulering af tæller- og nævnerdefinitioner, så det er helt tydeligt, hvad der skal inkluderes det ene og det andet sted, så Bente og Børge tæller på samme måde mandag morgen og lørdag nat.
Tip til praktisk dataindsamling og -behandling
I eksemplet med pneumonipatienter indsamler man data manuelt ved morgenkonferencen. Men hvis data allerede er tilgængelige i fx den elektroniske patientjournal, kan opgaven måske automatiseres. Bemærk, at data i dette tilfælde ikke behøver være personhenførbare, idet det er processerne omkring diagnostik og behandling, der er interessante – ikke den enkelte patient.
Når man samler data, skal man så vidt muligt undgå at bearbejde data allerede i indsamlingsøjeblikket. Man kunne i eksemplet have valgt blot at notere for hver patient, om behandlingen var rettidigt indledt (ja/nej). På den måde kunne dataindsamlingen måske gøres lidt enklere. Men samtidig ville man afskære sig selv for på et senere tidspunkt at opgøre data på andre måder.
Ved at dikotomisere grunddata, som det hedder, når man oversætter en kontinuert variabel (i dette tilfælde tid) til en logisk variabel (ja/nej), fjerner man information. Hvis man derimod indsamler grunddata så ubearbejdet som muligt, bliver det muligt sidenhen at opgøre data på flere forskellige måder. Det kan være, at ny evidens på et tidspunkt gør det interessant at vide, hvilken andel af patienterne, som kom i behandling inden for to, otte eller syvtrekvart timer. Det kan også være, man ønsker at se på tid til behandlingsstart for individuelle patienter eller den mediane eller gennemsnitlige tid for alle patienter per uge. Alle disse muligheder går tabt i det øjeblik, man allerede i dataindsamlingsøjeblikket reducerer data.
En beslægtet kunstfejl er at aggregere data allerede ved kilden. Dette sker ofte, når man samler data ved auditmetoden, hvor man gennemgår et antal patientforløb for en given tidsperiode. Det er fristende blot at notere tæller og nævner for hele perioden. Men ved at notere grunddata for det enkelte forløb, mangedobler man sine muligheder for at opgøre indikatoren på forskellige måder. I eksemplet ovenfor aggregerer man data efter, de er indsamlet. På den måde er det let, siden hen at ændre fx opgørelsesperiode fra uge til måned.
Særligt gælder det for tidsintervaller, at de kan være vanskelige eller umulige at ændre. Man kan ikke lave månedsopgørelser med ugedata og omvendt. Men hvis grunddata indeholder de eksakte datoer for det, man undersøger, kan man opgøre data i alle tænkelige tidsintervaller: dag, uge, to-, tre-, fire-ugersperiode, måned, kvartal osv.
Dette betyder dog ikke, at man aldrig skal reducere eller aggregere data allerede i indsamlingsøjeblikket. Der kan være særdeles gode grunde til at gøre det. Men man skal være bevidst om sin indsamlingsstrategi og nøje overveje fordele og ulemper ved den ene og den anden metode. En god grund til at aggregere data – ud over at lette dataindsamlingen – kan være at maskere personhenførbare data. På den måde slipper man for bøvl med tilladelser og krav til databasesystemer med logning osv. Særligt i tidsbegrænsede her og nu-projekter kan det betyde forskellen på succes og fiasko, om man skal vente på tilladelser til at gå i gang.
Sammenfattende kan man sige, at man skal tilstræbe så høj opløsning som muligt i sine grunddata under hensyntagen til dataindsamlingsresurser og behovet for maskering af personhenførbare oplysninger.
Case: Tid til grad 2-sectioPå fødeafdelingen på Hospitalsenhed Vest (Herning og Holstebro) arbejder man bl.a. med forløbstider ved akutte kejsersnit (case beskrevet i kapitel 11) Efter hvert kejsersnit noterer jordemoderen fødselstidspunkt, tidspunkt for ordination af kejsersnit samt i hvilken grad kejsersnittet var akut (grad 1-3). For hver akuthedsgrad er der en tidsgrænse, som man tilstræber overholdt for mindst 90% af kejsersnittene. For grad 2-kejsersnit er grænsen 30 minutter. Data omfatter i alt 354 grad 2-kejsersnit fra perioden januar 2016 til august 2019. Tabellen viser data for de første 6 kejsersnit.
Variablen datetime angiver fødselstidspunktet; month er fødselsmåned, som er beregnet ud fra datetime. Vi skal bruge fødselsmåneden til at aggregere data til P- og Xbar-diagrammer; sectio_delay er tiden (i minutter) fra ordination af kejsersnit til barnet er født. Af hensyn til beskyttelse af personoplysninger er der tilført støj til datetime-variablen, så fødselstidspunkterne i tabellen afviger fra de faktiske fødselstidspunkter. Fordi grunddata registreres for hvert enkelt kejsersnit, er det muligt at tilpasse sine opgørelser til forskellige målgrupper. Hospitals- og regionsledelsen ønsker måske blot at vide, om standarden bliver overholdt, og om overholdelsen er stabil. P-diagrammet viser, at 90% af kejsersnittene sker inden for tidsrammen, og at processen er stabil.
Afdelingens læger og jordemødre ønsker måske at kende den gennemsnitlige tid fra ordination af kejsersnit til fødsel. Det viser Xbar-diagrammet, hvor hvert målepunkt angiver den gennemsnitlige tid til kejsersnit i hver måned. Alle målepunkter ligger inden for kontrolgrænserne og omkring en gennemsnitstid på 23 minutter.
Data til P- og Xbar-diagrammerne fås ved at aggregere grunddata per måned. Tabellen ovenfor viser aggregerede data for de første seks måneder. Variablen n_ontime angiver antallet af grad 2-kejsersnit, som er udført inden for tidsgrænsen; n_sectio angiver det totale antal grad 2-kejsersnit; p_ontime angiver proportionen af kejsersnit udført til tiden og udgør datapunkterne i P-diagrammet; avg_delay angiver den gennemsnitlige tid til kejsersnit og udgør datapunkterne i Xbar-diagrammerne; og sd_delay angiver standardafvigelsen i tid til kejsersnit. Kontrolgrænserne i de to diagrammer udregnes ved at indsætte de relevante parametre i formlerne for hhv. P- og Xbar-diagrammet.
Forbedringsteamet, hvis opgave det er at skabe robuste processer og arbejdsgange, som sikrer den enkelte fødende højst mulig kvalitet, har brug for flere detaljer. Dem finder de i et I-diagram over individuelle forløbstider, hvor hvert målepunkt er forløbstiden for ét enkelt kejsersnit. I-diagrammet har (naturligvis) det samme gennemsnit på 23 minutter som Xbar-diagrammer, men viser tillige, at processen er ustabil på individniveau, idet enkelte kejsersnit tager usædvanligt lang eller kort tid. I-diagrammet viser også, at den nuværende proces ikke tillader 100%-gennemførsel inden for tidsgrænsen. Det fremgår ved, at øverste kontrolgrænse på 36 minutter er over tidsgrænsen på 30 minutter, som er angivet med den vandrette grønne streg.
Hvert diagram har sine styrker og svagheder, og de tre diagrammer viser tre sider af de samme data og besvarer i virkeligheden forskellige spørgsmål. Til administratorer og til offentligheden kan vi sige, at vi overholder standarden og holder et stabilt niveau, dvs. det går godt. Til os selv kan vi sige, at der er plads til forbedring i form af stabilisering af individuelle forløbstider. Hvis vi kan identificere årsagerne til de kejsersnit, som befinder sig uden for kontrolgrænserne og dermed skiller sig ud på den gode eller den dårlige måde, kan vi udover at stabilisere processen måske endda reducere den gennemsnitlige forløbstid. Endelig kunne vagtplanlæggeren af hensyn til planlægning af den fremtidige bemanding i vagterne måske ønske at vide, om antallet af kejsersnit er stabilt og forudsigeligt fra måned til måned. Dette spørgsmål kan besvares med et C-diagram over det månedlige antal kejsersnit.
C-diagrammet viser særlig variation i form af et skift med en usædvanligt lang serie på ni datapunkter mod forventet højst otte til sidst på kurven. Noget kunne altså tyde på, at der er begyndt at komme færre kejsersnit. Dette bør undersøges nærmere. Der kan være mange forklaringer. En forklaring kunne være, at faldet skyldes bevidste tiltag for at reducere hyppigheden af kejsersnit. Dette ville formentlig være en positiv udvikling. Det kunne også være, at man af den ene eller anden grund var begyndt at foretage flere elektive kejsersnit og dermed færre akutte, eller at fødselstallet simpelthen var faldet. Man må overlade det til fagfolk med godt lokalkendskab at afgøre, om skiftet er ønsket, uønsket eller ligegyldigt. Uanset hvad, vil det være fornuftigt at lede efter en forklaring. |
Case: Sjældne kirurgiske infektionerVi kalder det sjældne hændelser, når det, vi tæller, sker så sjældent, at vi ikke kan samle nok data til, at SPC-diagrammet giver mening. Det viser sig ved, at selv måneds- eller kvartalsopgørelser (for) ofte indeholder nul defekte(r). “Sjælden” er et relativt begreb. På hospitalsniveau er hospitalsinfektioner sjældent sjældne – en om dagen på Rigshospitalet. Men den lille afdeling eller den enkelte læge oplever måske kun en enkelt eller slet ingen hospitalsinfektioner på et helt år. I seriediagrammet nedenfor er medianen nul, fordi mere end halvdelen af målepunkterne er nul. Derfor giver det ikke mening at lede efter lange serier og få kryds; der er kun én serie og ingen kryds.
P-diagrammet er mere brugbart, men tallene er stadig så små og kontrolgrænserne derfor så brede, at det ville tage lang tid for os at opdage hvis infektionshyppigheden skulle ændre sig markant. Der skal ske en mangedobling af infektionsrisikoen, før kurven krydser den øvre kontrolgrænse. Og, fordi nedre kontrolgrænse er censureret ved nul, skal der gå mange måneder uden infektioner, før vi opdager en reduktion i infektionsrisikoen.
Når hændelser bliver så sjældne, at de ikke kan opgøres meningsfuldt i passende tidsintervaller på x-aksen, kan man i mange tilfælde slippe af sted med at omdefinere indikatoren – vende den om så at sige – så man i stedet for at tælle antal hændelser per tidsenhed tæller tiden mellem hændelser. På afdelingen kan man fx tælle antal dage mellem nyopståede infektioner eller andre uønskede hændelser. Kirurgen vil måske tælle antal operationer mellem postoperative komplikationer. Og medicineren kan tælle, hvor mange patienter, der overlever et AMI mellem hvert AMI-relateret dødsfald. Til disse typer indikatorer findes såkaldte T- og G-diagrammer. T for tid mellem hændelser (fx dage mellem infektioner) og G for ikke-defekte enheder mellem defekte enheder (fx operationer mellem komplikationer) (Benneyan 2002). G-diagrammet nedenfor viser, at der mediant går 156 operationer mellem, der opstår en infektion, og at en sikker forbedring (= færre infektioner) vil vise sig den dag, der går op mod 1000 operationer mellem infektioner.
Bemærk, at fordi G-diagrammet baserer sig på antagelser om, at data følger den geometriske sandsynlighedsfordeling, som er stærkt asymmetrisk, bruger man som regel medianen som midtlinje. På den måde kan man stadig applicere test for lange serier og få kryds, som i sagens natur forudsætter at data er nogenlunde symmetrisk fordelt om midtlinjen. G-diagrammet er dog ingen mirakelkur mod sjældne hændelser. Bemærk, at der skal gå op til 1000 operationer mellem infektioner, før vi krydser øvre kontrolgrænse. Med i gennemsnit 75 operationer om måneden, betyder det, at der skal gå over et år uden infektioner, før vi kan være sikre på, at risikoen reelt er reduceret. I P-diagrammet ovenfor skal vi kun vente ni måneder, før vi har en usædvanlig lang serie under midtlinjen. Man skal også være opmærksom på, at G-diagrammet sjældent har nogen nedre kontrolgrænse og derfor er uegnet til at opdage forværringer, som viser sig ved, at kurven går nedad. I virkeligheden supplerer P- og G-diagrammerne hinanden, og man kan med fordel vise dem sammen. Det er min erfaring, at det er hip som hap, hvilket af de to, som først signalerer, når processen skifter. |
Håndværk, Videnskab og Tankegang
SPC er på samme tid et håndværk og en videnskab – men først og fremmest er SPC en tankegang (Wheeler 2000). Håndværket og videnskaben kan man træne og læse sig til. Det svære er at tilegne sig tankegangen.
SPC-tankegangen er tydeligst udtrykt i Tabel 1 med de fire tilstande og tilhørende handlinger. Den kan man jo hurtigt læse op på. Men det kræver tid og øvelse at internalisere den. Til gengæld er udbyttet besværet værd. For den kvalitetsbevidste organisation er SPC det sunde alternativ til skiftende bevidstløse og skadelige indgreb i stabile processer og blind tiltro til ustabile processer på afveje.
SPC har siden sin fødsel for snart 100 år siden revolutioneret produktionsindustrien verden over. I sundhedsvæsenet og andre servicebrancher er det gået noget langsommere. Selv om mange klinikere og kvalitetsmedarbejdere har taget SPC til sig, kan det tælles på et par fingre de steder, hvor SPC er integreret fra top til bund i hele ledelses- og produktionssystemet.
Vi håber, at dette kapitel kan være med til at udruste fremtidens klinikere og ledere, så SPC får den plads i sundhedsvæsenet, som patienterne (det er også os) fortjener.
Hyppigt stillede spørgsmål
Hvor mange data er nødvendige til et SPC-diagram?
Kort sagt: der går 20-30 målepunkter til et godt SPC-diagram. Er der færre risikerer man i højere grad at overse særlig variation. Er der flere risikerer man flere falske signaler. Dette betyder ikke, at flere eller færre målepunkter ikke kan bruges. Man skal naturligvis udnytte de data, man har, blot man er opmærksom på betydningen af antallet af datapunkter for fortolkningen.
I kejsersniteksemplet ovenfor er der 354 datapunkter i I-diagrammet. I fortolkningen bør man derfor være opmærksom på den forøgede risiko for falske signaler, som findes, når der er så mange datapunkter. I eksemplet kan det måske betale sig at “nøjes” med at undersøge de tre datapunkter, der ligger længst fra kontrolgrænserne. Der er formentlig i dem, man finder den vigtigste læring om, hvad der en gang i mellem går særligt galt og godt.
Hvor hyppigt skal jeg måle?
Det giver sig selv, at hvis man skal bruge 20-30 datapunkter til et godt SPC-diagram, så er der ikke meget kvalitetsudvikling at hente i års- og kvartalsdata. Selv med månedlige data, vil der gå op til to år, før vi med sikkerhed kan afgøre, om processen er stabil eller ej. Man skal altså måle hyppigt.
En anden god grund til at måle hyppigt er det, der i fagsproget kaldes rational subgrouping, som betyder noget i retning af fornuftig inddeling af x-aksen. For at maksimere chancerne for at opdage særlig variation, skal man måle hyppigt nok til, at eventuelle skift vil forekomme mellem målepunkterne. Eller med andre ord: målefrekvensen skal være højere end forandringsfrekvensen. Hvis man fx forventer, at forandringer kan ske fra uge til uge, skal man måle dagligt eller i det mindste ugentligt.
Omvendt risikerer man ved hyppige målinger, at tallene i datapunkterne bliver for små. Dette gælder for tælletal og medfører, at den tilfældige variation (støjen) fra målepunkt til målepunkt bliver større og dermed lettere kommer til at maskere eventuelle signaler. Som en grov tommelfingerregel kan man tilstræbe, at der i gennemsnit er mindst 4-5 defekte eller defekter i tælleren i hvert målepunkt.
Så på den ene side skal man måle hyppigt nok til, at eventuelle forandringer sker mellem målepunkterne og på den anden side så sjældent, at datapunkterne indeholder nok data.
Er det nødvendigt at have baseline-data før et forbedringsprojekt går i gang?
Det bedste udgangspunkt for et kvalitetsudviklingsprojekt er en god, solid baseline, som med 20-30 målepunkter viser stabil proces. Et godt eksempel er C. difficile-casen fra før. I sådanne tilfælde, kan man fastlåse midtlinjen og eventuelle kontrolgrænser og forlænge dem ud i fremtiden. Når midtlinje og grænser er låst, vil man hurtigere opdage eventuelle skift i data.
Men hvad gør man, hvis man ikke har data til en god, solid baseline? Skal man vente med at forbedre kvaliteten, til man har etableret en baseline, eller skal man bare gå i gang? Svaret kommer an på situationen.
Hvis man har et erkendt og alvorligt problem i sin afdeling, kan man selvfølgelig ikke vente halve eller hele år på en baseline. Så må man i gang med at forbedre kvaliteten med det samme, og indikatormålingerne må følge med, så godt de kan. Det er min erfaring, at de færreste udviklingsprojekter virker med det samme. Det betyder, at man alligevel næsten altid opnår en form for baseline i løbet af det første stykke tid, mens man afprøver sine forandringsideer.
Omvendt, hvis man blot har en fornemmelse af, at noget kunne gøres bedre, uden at det er livet om at gøre, at det sker her og nu, kan man måske godt forsvare at tage den nødvendige tid til at belyse problemet og udviklingsmulighederne grundigt med en SPC-analyse af en omhyggeligt udført baselineregistrering.
Hvornår er det fornuftigt at opdele SPC-diagrammet i flere perioder?
I C. difficile-casen (i afsnittet ’Serie- og/eller kontroldiagrammer – hvad skal du vælge?’) opdelte vi diagrammet i to perioder før og efter interventionen. På den måde er det let på øjemål at kvantificere forskellen på perioderne. Men før man opdeler sit diagram, skal man sikre sig, at forudsætninger for en opdeling er opfyldt. Når man opdeler et diagram, vil man næsten med garanti få forskellige midtlinjer i de forskellige perioder – også selv om der ikke er sket væsentlige ændringer i de underliggende processer. Det kan snyde læseren til at tro, at der er sket forbedringer (eller forværringer). Denne praksis er udbredt – også i den “finere” litteratur og på videnskabelige kvalitetskonferencer – men den er ikke desto mindre forkert.
Det kan være nyttigt at opdele et SPC-diagram når
- der er et tydeligt skift i data,
- årsagen til skiftet er kendt,
- den nye proces er bedre end den gamle, og
- vi forventer, at den nye proces fortsætter.
Hvis blot én af betingelserne ikke er opfyldt, skal man hellere bruge sin tid på at afprøve ideer til arbejdsgange, den kan stabilisere og/eller forbedre processen.
Hvorfor alt det besvær med serie- og kontroldiagrammer?
Kan vi ikke bare sammenligne kvaliteten før og efter en indsats med fx t- eller chi i anden-test?
Sagtens. Blot man sikrer sig, at både før- og efter-perioden hver for sig er statistisk stabile, dvs. kun rummer almindelig variation. Er de ikke det, er forudsætningerne for komparative analyser af gennemsnit og proportioner ikke opfyldt. Det giver ingen mening at sammenligne gennemsnit fra to processer, som er i bevægelse. Det ville svare til at sammenligne gennemsnitshastigheden hos en bil, der accelererer med gennemsnitshastigheden hos en bil, der bremser.
Man kan undersøge før- og efter-perioderne for særlig variation ved at placere dem i et SPC-diagram. Og hvis man gør det, er det slet ikke nødvendigt med t- eller chi i anden-test.
Hvor finder jeg SPC-software?
Man kan komme rigtig langt med hardware i form af papir og blyant. Det kræver få statistiske kundskaber at tegne og fortolke et seriediagram. Og de fleste kan hurtigt lære at udregne kontrolgrænser til et I-diagram.
Men meget bliver naturligvis lettere, hvis man har en computer til at hjælpe sig. Alle de store statistikprogrammer som SAS, JMP, STATA, SPSS og R indeholder moduler, som kan lave kontroldiagrammer. Til Excel kan man købe forskellige plug ins, som kan lave SPC-diagrammer. Man kan også relativt let lave sine egne regnearksskabeloner til formålet. Endelig er der EpiData, som er et dansk udviklet statistikprogram, der også kan lave SPC-diagrammer.
Aktuelt (pr. medio 2021) findes skift og kryds-reglerne kun i qicharts2-pakken til R (Anhøj 2018, 2019). De andre programmer benytter forskellige udgaver af Western Electric-reglerne, og de færreste kan lave seriediagrammer. Både qicharts2 og R er open source og gratis. De andre programmer er dyre, medmindre man er studerende. Undtagelsen er EpiData, som er gratis til personligt brug, men som man forventes at betale for eller på anden måde bidrage til, hvis man bruger det til arbejds- eller kommercielle formål.
qichart2 forudsætter, at man behersker R til husbehov. R er (ligesom SAS og STATA) et programmeringssprog, som det tager tid at lære. Men har man først lært det, er der ingen grænser for, hvad R i øvrigt kan bruges til – ikke mindst i hænderne på læger, som skal forske og kvalitetsudvikle resten af livet. Kort sagt: Læge, lær R!
Hvor finder jeg gode data til mit kvalitetsudviklingsprojekt?
Det er sjældent, at gode data til kvalitetsudvikling findes på forhånd – i hvert fald i tilstrækkeligt omfang. Man kan finde mange gode data i de elektroniske journalsystemer, i Landspatientregisteret og i de kliniske kvalitetsdatabaser (se også Datakilder, der kan bidrage til analyser af kvaliteten – link til underside til kapitel 2). Men det er sjældent, sådanne data er tilstrækkelige til at drive konkrete kvalitetsudviklingsprojekter.
I eksisterende datakilder finder man især data, som er brugbare til at konstruere resultatindikatorer. Fx stammer rådata om hospitalsinfektioner i ovenstående eksempler fra mikrobiologiske databaser og Landspatientregisteret. Men eksisterende datakilder er næsten altid utilstrækkelige til at konstruere procesindikatorer. I kejsersniteksemplet samler jordemødrene på Hospitalsenhed Vest selv data ind efter hver fødsel. I journalsystemet findes nemlig ikke pålidelige oplysninger om tidspunkt for ordination af kejsersnit. Faktisk samler jordemødrene mange flere data om den enkelte fødsel til brug for deres lokale kvalitetsarbejde – afhængig af fødselstype noterer de op til over 100 variable i en til formålet oprettet database. De har udviklet en arbejdsgang, hvor denne efterregistrering kan overstås på mindre end fem minutter, hvilket i sig selv er imponerende.
Hvorfor ikke 2 sigma?
Fra al anden statistik har vi vænnet os til, at det normale skal findes inden for +/- 2 sigma fra gennemsnittet. Så hvorfor bruger man 3 sigma i kontroldiagrammer?
Det er let at argumentere statistisk for, at 3 sigma er en bedre afgrænsning af almindelig variation i kontroldiagrammer end 2 sigma. Men læs svaret til ende, før du køber forklaringen.
Kontroldiagrammer er i realiteten gentagne (20-30) statistiske test. Med tilfældige, normalfordelte data er chancen for, at det enkelte datapunkt falder uden for 2 sigma ca. 5%. Men i et kontroldiagram gentager vi testen mange gange. Med 20 datapunkter fra en stabil proces med normalfordelte data er sandsynligheden for, at alle datapunkterne ligger mellem +/- 2 sigma = 1 - 0.9520 = 0.64. Det betyder, at hvis vi lader 2 sigma-grænser være afgørende for, om processen er stabil eller ej, skal vi forberede os på, at en tredjedel af vores kontroldiagrammer indeholder et eller flere falske signaler. Med 3 sigma er sandsynligheden for, at en tilfældig måling falder uden for 0.03%, og nu ser regnestykket mere fornuftigt ud: 1 - 0.99720 = 0.06.
Shewhart havde naturligvis selv gjort sig disse overvejelser. Men det er interessant, at han protesterede flere gange i både skrift og tale mod denne statistiske forklaring: In other words, the fact that the criterion we happen to use has a fine ancestry of highbrow statistical theorems does not justify its use. Such justification must come from empirical evidence that it works. (Shewhart 1931, p. 18)
Shewhart valgte altså 3 sigma til sine kontrolgrænser af den simple grund, at de fungerer i praksis. Der er i de 100 år, der snart er gået, gjort mange forsøg på at finde bedre kontrolgrænser; men 3 sigma står stadig ubesejret.
Referencer
———. 2018. “qicharts2: Quality Improvement Charts for R”. JOSS. .
———. 2019. qicharts2: Quality Improvement Charts for R.
Anhøj, Jacob, og Anne-Marie Blok Hellesøe. 2016. “The problem with red, amber, green: the need to avoid distraction by random variation in organisational performance measures”. BMJ Qual Saf. .
Anhøj, Jacob, og Anne Vingaard Olesen. 2014. “Run Charts Revisited: A Simulation Study of Run Chart Rules for Detection of Non-Random Variation in Health Care Processes”. PLoS ONE.
Anhøj, Jacob, og Tore Wentzel-Larsen. 2018. “Sense and sensibility: on the diagnostic value of control chart rules for detection of shifts in time series data”. BMC Medical Research Methodology.
Benneyan, James. 2002. “Number-Between g-Type Statistical Quality Control Charts for Monitoring Adverse Events”. Health care management science 4 (januar): 305–18.
Carstensen, Jeppe West, Mahtab Chehri, Kristian Schønning, Steen Christian Rasmussen, Jacob Anhøj, Nina Skavlan Godtfredsen, Christian Østergaard Andersen, og Andreas Munk Petersen. 2018. “Use of prophylactic Saccharomyces boulardii to prevent Clostridium difficile infection in hospitalized patients: a controlled prospective intervention study”. Eur J Clin Microbiol Infect Dis 37: 1431–9.
Montgomery, Douglas C. 2009. Statistical Quality Control: A Modern Introduction, sixth ed. John Wiley & Sons.
Quality America Inc. 2016. “Tampering”. 2016.
Shewhart, Walther A. 1931. Economic control of quality of manufactured product. New York: D. Van Nostrand Company.
Western Electric Company. 1956. Statistical Quality Control Handbook. New York: Western Electric Company inc.
Wheeler, Donald J. 2000. Understanding Variation – The Key to Managing Chaos, third ed. SPC Press.
Bogens teoretiske grundlag
Denne håndbog handler om det, man kalder ’forbedringsarbejde’ (efter det amerikanske ’improvement’-begreb), ’implementering’ eller ’kvalitetsudvikling’.
Implementering, kvalitetsudvikling, forbedringsarbejdeDen proces, der skal til, for at evidensbaseret viden om udredning, pleje og behandling kommer alle relevante patienter til gode, kan kaldes ’implementering’. Andre begreber om det samme er ’kvalitetsforbedring’, ’kvalitetsudvikling’ eller ’forbedringsarbejde’. I denne bog bruges disse begreber synonymt. |
Der findes en række ’skoler’ eller tilgange inden for implementering, der har det til fælles, at de beskriver teorier, metoder og begreber, der tilsammen udgør en praktisk tilgang til at forbedre arbejdsgange. Udgangspunktet i denne bog er ’model for improvement’. Andre tilgange er fx ’lean’, ’six sigma’ eller ’productive ward’ (1).
De respektive tilgange adskiller sig en del – særligt ved den kultur de indirekte søger at skabe. Skal man forbedre kvaliteten vha. tavlemøder, data eller afprøvninger? Men sammenligner man de forskellige tilgange på tværs, så har de flere ligheder end forskelle:
- De fokuserer på samtidig at skabe bedre sundhed for en gruppe (fx færre skader, mere relevant behandling eller kortere ventetid), bedre oplevelser for ’kunden’ (fx patienten) og med lavere omkostninger for samfundet. Dette kaldes tilsammen ’the triple aim’ (2).
- De baserer sig på en videnskabelig tilgang til at forstå processer og resultater.
- De tager udgangspunkt i et tydeligt formuleret mål, så man ved, hvornår man kan kalde noget en succes.
- Tilgangene har fokus på brug af tidstro data, der anvendes i stikprøver store nok til at vurdere om processen går i den rigtige retning.
- De tager udgangspunkt i, at ideerne til at forbedre noget skal komme fra dem, der er en del af systemet eller fra dem som oplever kvaliteten på egen krop fx medarbejdere, patienter eller pårørende.
- Tilgangene har et fælles fokus på at pilotteste eller afprøve i lille skala og løbende udvikle arbejdsgangen systematisk indtil man har en model, der gør det let at gøre det rigtigt.
- Tilgangene tilskriver ledelserne en særlige rolle med at bakke op om kvalitetsprojektet, sætte tydelige mål, efterspørge resultater og fjerne barrierer – med respekt for medarbejdernes ideer, dataindsamling og afprøvninger.
Målet med håndbogen er at beskrive overnævnte punkter med udgangspunkt i Model for Improvement, forbedringsmodellen. Det er en af de metoder, der også anvendes i de såkaldte lærings- og kvalitetsteams (LKT) i Det National Kvalitetsprogram (3).
Andre kapitler i bogen handler om, hvordan du som læge rent praktisk kan gribe forbedringsarbejdet an, hvordan du skaffer dig opbakning i organisationen, og hvordan du kan være med til at sprede gode resultater af forbedringsarbejdet til større dele af organisationen fx en afdeling, et hospital eller et speciale.
Bogen giver også bud på, hvordan forbedringstankegang og udbredelse af viden om løbende tilpasning af arbejdsgangene kan blive en integreret del af lægernes hverdag.
Yderligere et kapitel handler om, hvordan man publicerer resultater af systematisk implementering, hvorved man både kan dele erfaringerne med andre og få formel anerkendelse for det, man har gennemført.
Som tillæg findes et særligt kapitel om statistisk proceskontrol (SPC), der er et nyttigt statistisk værktøj i forbindelse med kvalitetsudvikling.
Referencer
- Scoville R, Little K. Comparing Lean and Quality Improvement. IHI White Paper. Cambridge, Massachusetts: Institute for Healthcare Improvement; 2014. (Available at ihi.org) (tilgået sept 2021).
- Berwick DM, Nolan TW, Whittington J. The triple aim: care, health, and cost. Health Aff (Millwood). 2008 May-Jun;27(3):759-69. doi: http://doi.org/10.1377/hlthaff.27.3.759. PMID: 18474969.
- https://kvalitetsteams.dk/laerings-og-kvalitetsteams/om-laerings-og-kvalitetsteams (tilgået sept 2021).
Manifest
Ideen til håndbogen "Læge - kend din kvalitet" opstod på et møde i Lægeforeningen i 2018, hvor en gruppe læger underskrev et manifest, læger for Databaseret Kvalitetsudvikling.
Manifest, Læger for databaseret kvalitetsudvikling, Domus Medica 5. februar 2018
- Vi anvender data til at træffe beslutninger, for at forbedre kvaliteten af patientbehandlingen.
- Før vi anvender data, vil vi forstå, hvordan og med hvilket formål data er opstået, indsamlet, behandlet og analyseret.
- Vi anerkender, at data varierer, og at to målinger af det samme sjældent er ens. Nogle forskelle i data skyldes tilfældig variation. Andre forskelle skyldes grundlæggende forandringer i de strukturer og arbejdsgange, som har skabt data.
- Vi præsenterer data, så det er tydeligt, hvilke forskelle, som må tilskrives tilfældig variation og hvilke forskelle, som kan tilskrives ikke-tilfældige forandringer.
- Vi præsenterer data, så væsentlig information i grunddata bevares.
- Vi præsenterer data uden at tilføre information, som ikke har belæg i grunddata.
- Vi anerkender, at kvalitetsforbedring er undervejs, når data viser ikke-tilfældig variation i den ønskede retning som følge af bevidste og målrettede forandringer af strukturer og arbejdsgange.
- Vi anerkender, at kvalitetsforbedring er opnået, når data viser tilfældig variation på et bedre niveau end tidligere.
Underskrevet af:
Andreas Rudkøbing, Ann Lyngberg, Christian von Plessen, Henriette Lipczak, Jacob Anhøj, Jens Winther Jensen, Kristian Antonsen, Louise Rabøl, Mark Krasnik, Stig Ejdrup Andersen, Vibeke Rischel
Uddybning af de enkelte punkter:
Vi anvender data til at træffe beslutninger, for at forbedre kvaliteten af patientbehandlingen
Kvalitetsforbedring forudsætter forandring, men ikke alle forandringer medfører forbedring. Kun med data kan vi vide, om der er behov for forbedring; og kun med data kan vi vide, om de forandringer, vi skaber, medfører forbedring. Før vi anvender data, vil vi forstå, hvordan og med hvilket formål data er opstået, indsamlet, behandlet og analyseret.
Før vi anvender data, vil vi forstå, hvordan og med hvilket formål data er opstået, indsamlet, behandlet og analyseret
Data forstås kun i den kontekst, de er opstået. Her er fx nogle data: 0,108 M 182 blå 54. Isoleret set har disse data ingen mening. Først når de forbindes, placeres i kontekst og tilføres måleenheder og definitioner forstår vi, at de beskriver en 54-årig mand, som vejer 108 kg, er 182 cm høj og har blå øjne. Hvis data skal bruges som beslutningsgrundlag, må vi vide mere, fx hvornår data er indsamlet, og om vægten er stabil eller under forandring.
Vi anerkender, at data varierer, og at to målinger af det samme sjældent er ens
Nogle forskelle i data skyldes tilfældig variation. Andre forskelle skyldes grundlæggende forandringer i de strukturer og arbejdsgange, som har skabt data.
Det er lige så menneskeligt som forkert at tillægge enhver forskel i data selvstændig betydning. Hvis den gennemsnitlige ventetid på behandling på de ene sygehus er 12,7 og på det andet 14,3 dage, er det naturligt at fremhæve det første sygehus som det bedste. Men selv, hvis de to sygehuse var ens, hvad angår størrelse og patientsammensætning mv., er denne fortolkning meningsløs uden kendskab til den naturlige variation i data.
Kun hvis forskellen overstiger den naturlige, tilfældige variation, og kun hvis de to tal kommer af stabile processer, hvis niveau ikke har ændret sig væsentligt over længere tid, kan forskellen tillægges betydning. At sammenligne to måleværdier uden at forholde sig til datas naturlige variation, er lige så meningsløst, som at fremhæve den person, der kaster en mønt og får krone, for den, som får plat.
Vi præsenterer data, så det er tydeligt, hvilke forskelle, som må tilskrives tilfældig variation og hvilke forskelle, som kan tilskrives ikke-tilfældige forandringer
Datadrevne beslutninger forudsætter prædiktion, som igen forudsætter stabilitet. Kun processer, som alene udviser tilfældig variation, er stabile og dermed forudsigelige.
Derfor bør præsentation af data til kvalitetsudvikling begynde med, at data placeres i et kurvediagram, som viser datas udvikling over tid. Markante udsving og betydende tendenser er lette at identificere med det blotte øje. Objektive test for mindre tydelige tegn til ikke-tilfældig variation fås ved at placere data i serie- og/eller kontroldiagrammer.
Vi præsenterer data, så væsentlig information i grunddata bevares
Med ”væsentlig information” menes i denne sammenhæng først og fremmest den rækkefølge data er fremkommet i. Hvis fx sygeplejersken kalder lægen med følgende besked: ”patientens temperatur har været 37, 38, 39 og 40 grader”, vil lægen (forhåbentlig) tilse patienten. Hvis samme data blev præsenteret som ”temperaturen har været 38, 40, 39 og 37 grader”, er det ikke til at sige, hvordan lægen vil reagere. Sygeplejersken siger ikke noget forkert, men den information, der findes i målingernes rækkefølge er væk, hvilket gør prædiktion og dermed fornuftig beslutning umulig.
Kun når data kommer af en stabil proces, er rækkefølgen ligegyldig. Men for at afgøre, om processen er stabil, må man kende rækkefølgen.
Sygeplejersken i eksemplet kunne også vælge at præsentere et sammendrag af data: ”Patienten har en gennemsnitstemperatur på 38,5 grader.” Igen er oplysningen korrekt men uegnet som beslutningsgrundlag. Kun ved stabile processer er det meningsfuldt at aggregere data.
Vi præsenterer data uden at tilføre information, som ikke har belæg i grunddata
Kvalitetsdata bliver ofte præsenteret i form af trafiklys og rangordninger, som har til formål at gøre det let at overskue store datamængder og hurtigt udpege de ”gode”, de ”onde” og de ”grusomme”. Trafiklys og rangordninger kan være nyttige til netop dette formål, forudsat at man i analysen forholder sig til typen og størrelsen af variation i data.
Kun data, som kommer af stabile processer, lader sig meningsfuldt udtrykke i farvekoder. Og kun når forskelle mellem hver for sig stabile processer overstiger den tilfældige variation, er det meningsfuldt at rangordne data og erklære noget for bedre eller dårligere end noget andet.
Vi anerkender, at kvalitetsforbedring er undervejs, når data viser ikke-tilfældig variation i den ønskede retning som følge af bevidste og målrettede forandringer af strukturer og arbejdsgange
I en stabil proces vil i gennemsnit hver anden måling være ”bedre” eller ”dårligere” end den foregående, uden at dette kan tages til indtægt for, at processen som helhed er under forbedring eller forværring. Det er overordentlig udbredt i fx års- og kvartalsrapporter, at lade sådanne tilfældige udsving i data danne grundlag for håndfaste konklusioner og beslutninger om ændringer af strukturer og arbejdsgange. Denne praksis er skadelig og kaldes i fagsproget tampering. Konsekvenserne af tampering er øget variation og dermed dårligere kvalitet.
Kun når en proces som helhed viser ikke-tilfældig variation med en tydelig retning mod forbedring, kan man tillade sig at konkludere, at forbedring er undervejs. Og kun når denne forbedring sker i tidsmæssig relation til kendte, tilsigtede ændringer, kan forbedringen tilskrives disse.
Vi anerkender, at kvalitetsforbedring er opnået, når data viser tilfældig variation på et bedre niveau end tidligere
En anden udbredt kunstfejl er at tage en enkelt måling, som tilfældigt befinder sig på den ønskede side af en målsætning eller standard, til indtægt for, at målet nået. Den modsatte fejlslutning, at kvaliteten er utilfredsstillende blot fordi, en enkelt måling tilfældigvis befinder sig på den forkerte side, er lige så almindelig.
Et mål kan først siges at være opnået eller en standard overhold, når den stabile proces varierer tilfældigt på et tilfredsstillende gennemsnit og med en tilfredsstillende variationsbredde.
I den forbindelse er det vigtigt at være opmærksom på, at den tilfældige variationsbredde i indikatorer, som baserer sig på tælledata, alene afhænger af tællerens og en eventuel nævners størrelse. Et procenttal med 5 patienter i nævneren, vil helt naturligt svinge mere end et tal med 50 patienter i nævneren. Det er derfor i de fleste tilfælde nyttigt at benytte gennemsnitsniveauet over en længere stabil periode til at afgøre, om målet er nået og overholdt. Med data, som basere sig på måleværdier, fx ventetider, kan variationsbredden have selvstændig betydning, hvorfor det i disse tilfælde kan være nyttigt, også at inddrage denne i sin målformulering.
Om bogen og bidragsyderne
”Læge - kend din kvalitet” er blevet til i samarbejde mellem Regionernes Kliniske Kvalitetsudviklingsprogram (RKKP) og Dansk Selskab for Patientsikkerhed.
Formålet med håndbogen er at give lægerne de bedste forudsætninger for at engagere sig i kvalitetsudvikling i sundhedsvæsnet herunder at sikre at ny evidens kommer alle relevante patienter til gavn.
Ideen til håndbogen opstod på et møde i Lægeforeningen i 2018, hvor en gruppe læger underskrev et manifest, Læger for Databaseret Kvalitetsudvikling.
Læge, kend din kvalitet er målrettet læger og skrevet af læger, der selv har gennemført kvalitetsudviklingsarbejde.
Arbejdet med bogen er koordineret af en redaktionsgruppe bestående af
- Louise Rabøl, ledende overlæge, Øre-, Næse-, Hals- og Kæbekirurgisk Afdeling, Sjællands Universitetshospital
- Jens Winther Jensen, direktør, Regionernes Kliniske Kvalitetsudviklingsprogram
- Jacob Anhøj, overlæge, Diagnostisk Center, Rigshospitalet
- Charlotte Frendved, læge, faglig redaktør, Dansk Selskab for Patientsikkerhed
Redaktionsgruppen vil gerne sige en særlig tak for opbakningen til projektet til Inge Kristensen, direktør, Dansk Selskab for Patientsikkerhed.
Redaktionen ønsker at takke forfatterne for jeres tålmodighed og bidrag:
- Ann Lyngberg, ledende overlæge, ph.d., Arbejds- og Socialmedicinsk Afdeling, Holbæk Sygehus
- Jens Stubager Knudsen, overlæge, Bedøvelse og Intensiv, Sygehus Lillebælt
- Julie Mackenhauer, læge, PhD, Dansk Center for Klinisk Sundhedstjenesteforskning, Aalborg Universitet og Socialmedicinsk Enhed, Aalborg Universitetshospital
- Markus Fally, læge, ph.d., post.doc., Lungemedicinsk Afdeling, Bispebjerg og Frederiksberg Hospital
- Mads Koch Hansen, læge, rådgiver, ledelsescoach, selvstændig
- Ole Bredahl Rasmussen, overlæge, Gynækologisk-obstetrisk afdeling, Hospitalsenheden Vest, Herning
Redaktionsgruppen ønsker at takke alle, der i øvrigt har bakket op og bidraget herunder særligt:
- Arjen Peter Stoop, chefkonsulent, Dansk Selskab for Patientsikkerhed
- Bodil Elgaard Andersen, chefkonsulent, Dansk Selskab for Patientsikkerhed
- Birgitte Dalgaard, kommunikationskonsulent, RKKP's Videncenter
- Brian Bjørn, speciallæge, patientsikkerhedsekspert, Laerdal
- Charlotte Sander Andersen, jordemodersupervisor, Gynækologisk-obstetrisk afdeling, Hospitalsenheden Vest, Herning
- Charlotte Rasmussen, kommunikationskonsulent, RKKP’s Videnscenter
- Christian von Plessen, speciallæge, ph.d., seniorrådgiver, Lausanne
- Christian Vestergård, læge, Dansk Selskab for Patientsikkerhed
- Hanne Ellegaard Miang, chefkonsulent, Dansk Selskab for Patientsikkerhed
- Helen Bruun, kvalitetskoordinator, Medicinsk Afdeling, Vejle Sygehus
- Henriette Lipczak, vicedirektør, ph.d., bestyrelsesformand i DSKS
- Inge Ulriksen, chefkonsulent, Dansk Selskab for Patientsikkerhed
- Jannie Christina Frølund, klinisk sygeplejespecialist, Medicinsk Afdeling, Vejle Sygehus
- Kristian Antonsen, speciallæge, hospitalsdirektør
- Liv Nørregaard Skøtt, projektchef, Dansk Selskab for Patientsikkerhed
- Line Flindt, grafiker
- Rikke von Benzon Hollesen, chefkonsulent, Dansk Selskab for Patientsikkerhed
Sidst men ikke mindst ønsker redaktionsgruppen at takke patientsikkerheds- og forbedringseksperterne Beth Lilja, Vibeke Rischel, Annemarie Hellebek og Janne Lehmann for den oprindelige idé til håndbogen – og for stor inspiration gennem årene.